研究背景
慢性手部湿疹(Chronic Hand Eczema, CHE)是常见的慢性炎症性皮肤病之一,其核心特征为疼痛、瘙痒及慢性炎症,病因复杂且受多种因素影响。该疾病临床表现多样,具有特应性皮炎(AD)、接触性皮炎及银屑病的重叠特征,这使得诊断与治疗工作极具挑战性。目前,慢性手部湿疹的潜在免疫机制尚未完全明确,仍需进一步深入研究。
2026年1月24日,法国里昂第一大学、图卢兹大学、波尔多大学等多机构联合团队在Allergy上发表了题为“Integrated Clinical Trial and Molecular Profiling Reveals Immune Drivers of Chronic Hand Eczema”的研究论文。该研究纳入94例中重度CHE患者,开展2b期随机双盲安慰剂对照临床试验,按1:1分为度普利尤单抗组与安慰剂组,整合皮肤转录组、血清和皮肤蛋白质组及光谱流式细胞术等多组学数据,系统探究了CHE的混合免疫驱动机制及IL-4Rα阻断治疗的疗效,为CHE的个体化治疗选择提供了关键参考。

文章标题
实验设计
样本队列:94例对强效外用糖皮质激素治疗无效、病程≥6个月的中重度CHE患者,按1:1随机分为度普利尤单抗治疗组(n=47)与安慰剂对照组(n=47),开展16周临床试验。
技术方法:整合了皮肤转录组学、皮肤和血清蛋白质组学及光谱流式细胞术,从基因、蛋白及免疫细胞表型多层面,系统刻画皮肤屏障功能与免疫炎症状态。
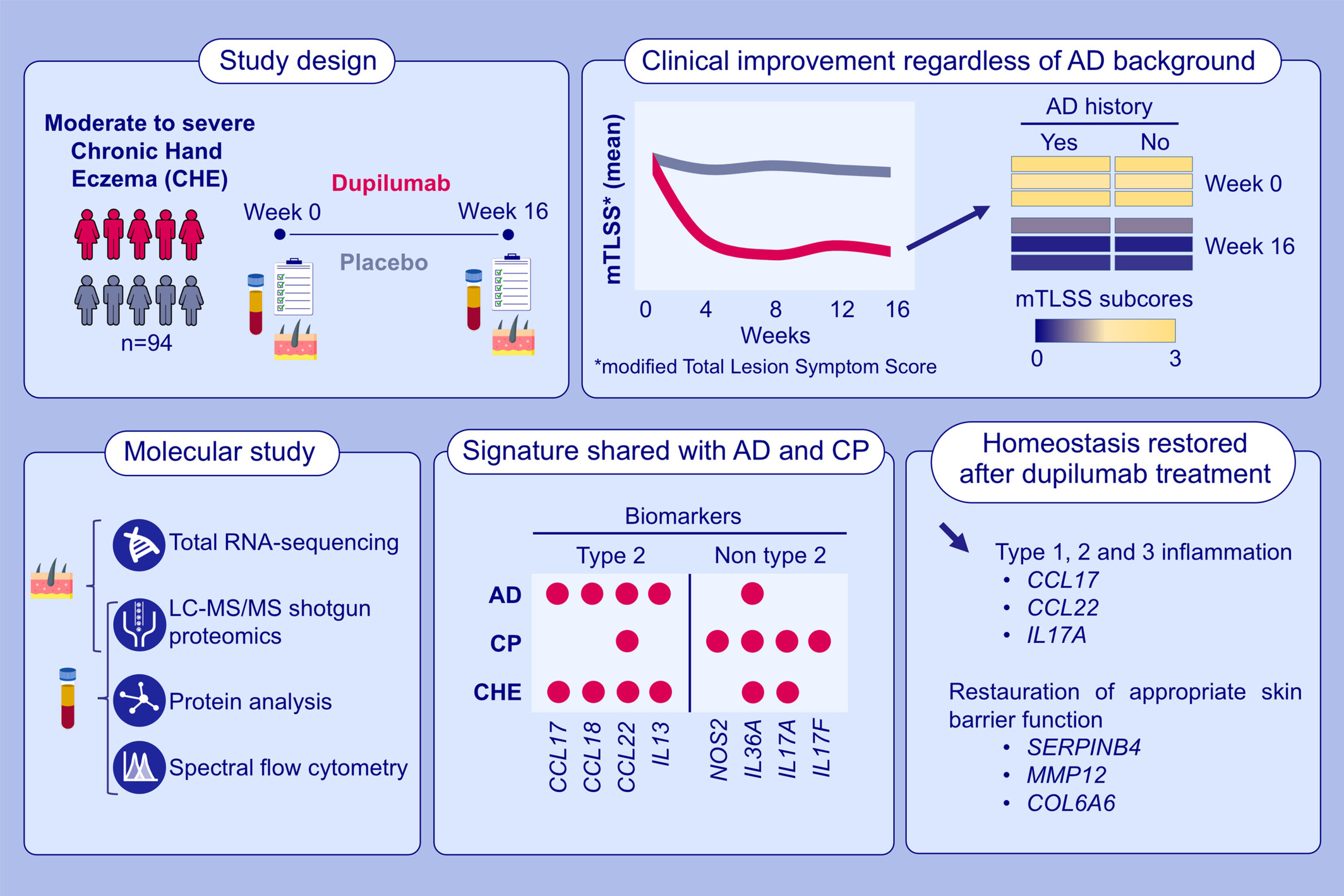
图形摘要
研究结果
01. CHE患者基线临床特征:异质性高,疾病负担显著
研究首先表明,特应性背景与临床表型是反映中重度CHE患者疾病负担的核心特征:有AD病史者更易合并过敏性鼻炎、哮喘等特应性疾病,且血清总IgE水平更高;临床表型以皲裂、角化过度为主,多表型叠加特征显著,76.6%患者双侧掌背同时受累。患者疾病平均病程8.72年,疾病负担随病程呈累积效应,基线mTLSS(改良皮损症状总评分)、DLQI(皮肤病生活质量指数)等指标显示其症状严重且生活质量受损显著,该特征在整合人口学、职业暴露等混杂因素后仍具稳定性(Fig. 1A),证实基线特征对CHE疾病评估具有独立参考价值。

Fig. 1 CHE患者基线临床特征
02. 度普利尤单抗治疗CHE疗效显著,且独立于AD背景
接下来,研究证实度普利尤单抗对中重度CHE的临床疗效显著优于安慰剂,且疗效独立于AD病史,为CHE广谱治疗提供关键证据。治疗16周后,度普利尤单抗组mTLSS平均改善59.8%,IGA、PaGA达清除或基本清除比例均超50%(Fig. 2A-D),患者瘙痒、疼痛等VAS评分及DLQI均显著改善(Fig. 2E-J),手部外湿疹症状也获缓解(Fig. 2L),且疗效经敏感性分析验证稳定;PCA分析显示,治疗干预是临床评分差异的关键因素,两组实现明显临床分层(Fig. 2K)。安全性上,两组不良事件发生率无显著差异,度普利尤单抗组以轻中度眼部不良事件为主,无严重不良事件致治疗中断,证实其用药安全性良好(Fig. 2L)。
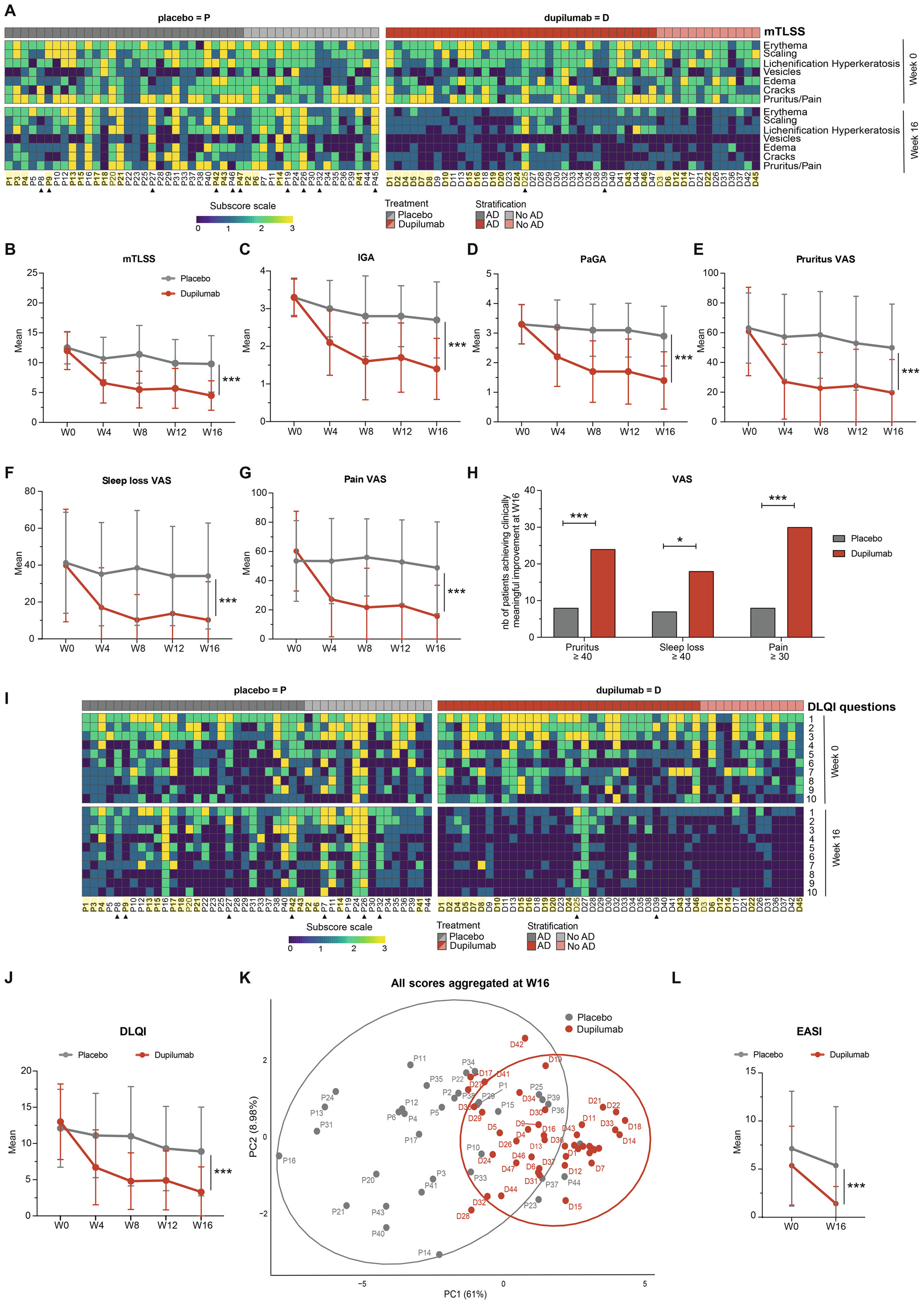
Fig. 2 度普利尤单抗治疗CHE疗效显著,且独立于AD背景
03. CHE的核心分子病理特征:混合免疫紊乱伴皮肤屏障损伤
研究证实,中重度CHE患者的皮肤转录组、血清蛋白质组特征与AD、银屑病高度重叠,存在1、2、3型混合免疫紊乱,同时伴随皮肤屏障功能相关基因和蛋白的异常调控。皮肤转录组显示,CHE患者与健康对照相比存在3552个下调、1913个上调差异表达基因(Fig. 3A-C),富集于角质形成细胞分化、白细胞介导的免疫和细胞因子信号传导等通路,高表达AD相关2型、银屑病相关3型及少量1型免疫标志物,其差异基因与AD、经典银屑病的重叠比例分别达34.1%-52%、36.4%-39%(Fig. 3F-G);血清蛋白质组分析显示,其2、3型免疫相关蛋白显著上调,与皮肤转录组特征一致(Fig. 3H-J)。另外,CHE患者循环B细胞数量增多、NK细胞、Th2及Th17细胞减少,皮肤免疫细胞浸润分析显示活化记忆CD4⁺T细胞、树突状细胞富集,同时皮肤屏障相关基因和蛋白表达异常,证实其皮肤屏障功能严重受损。
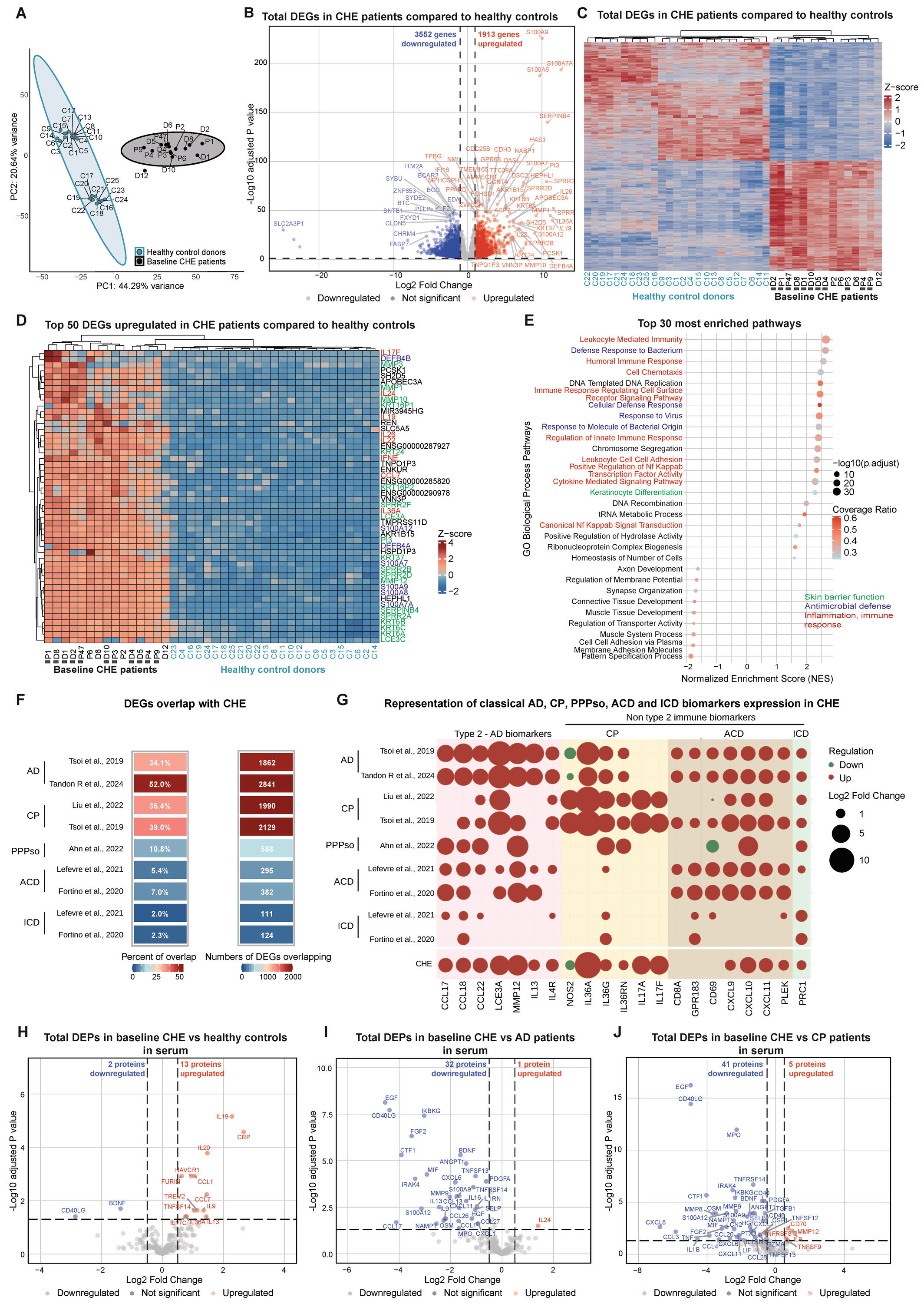
Fig. 3 CHE的核心分子病理特征:混合免疫紊乱伴皮肤屏障损伤
04. 度普利尤单抗的作用机制:修复皮肤屏障,重建免疫稳态
最后,研究证实度普利尤单抗通过阻断IL-4Rα信号,不仅抑制2型免疫通路,还可调节1、3型免疫反应,进而逆转CHE患者分子层面异常,恢复皮肤屏障功能并重建免疫稳态。皮肤转录组分析显示,治疗后出现491个差异表达基因,2/3为下调基因,涵盖1、2、3型免疫及组织重塑、应激角蛋白相关基因,疾病相关通路被显著抑制(Fig. 4A-E);与AD患者治疗转录组对比,二者共享44个以2型免疫、屏障相关基因为主的核心差异基因,CHE还存在特异性1、3型免疫调控基因(Fig. 4F-G)。蛋白质组分析表明,治疗后皮肤屏障相关蛋白表达恢复正常,血清中2、3型免疫相关蛋白显著下调,仅IL4因受体阻断特异性上调(Fig. 4H);皮肤免疫细胞组成推断分析显示活化树突状细胞、记忆CD4⁺T细胞浸润减少,而安慰剂组无上述分子修复效应(Fig. 4I)。
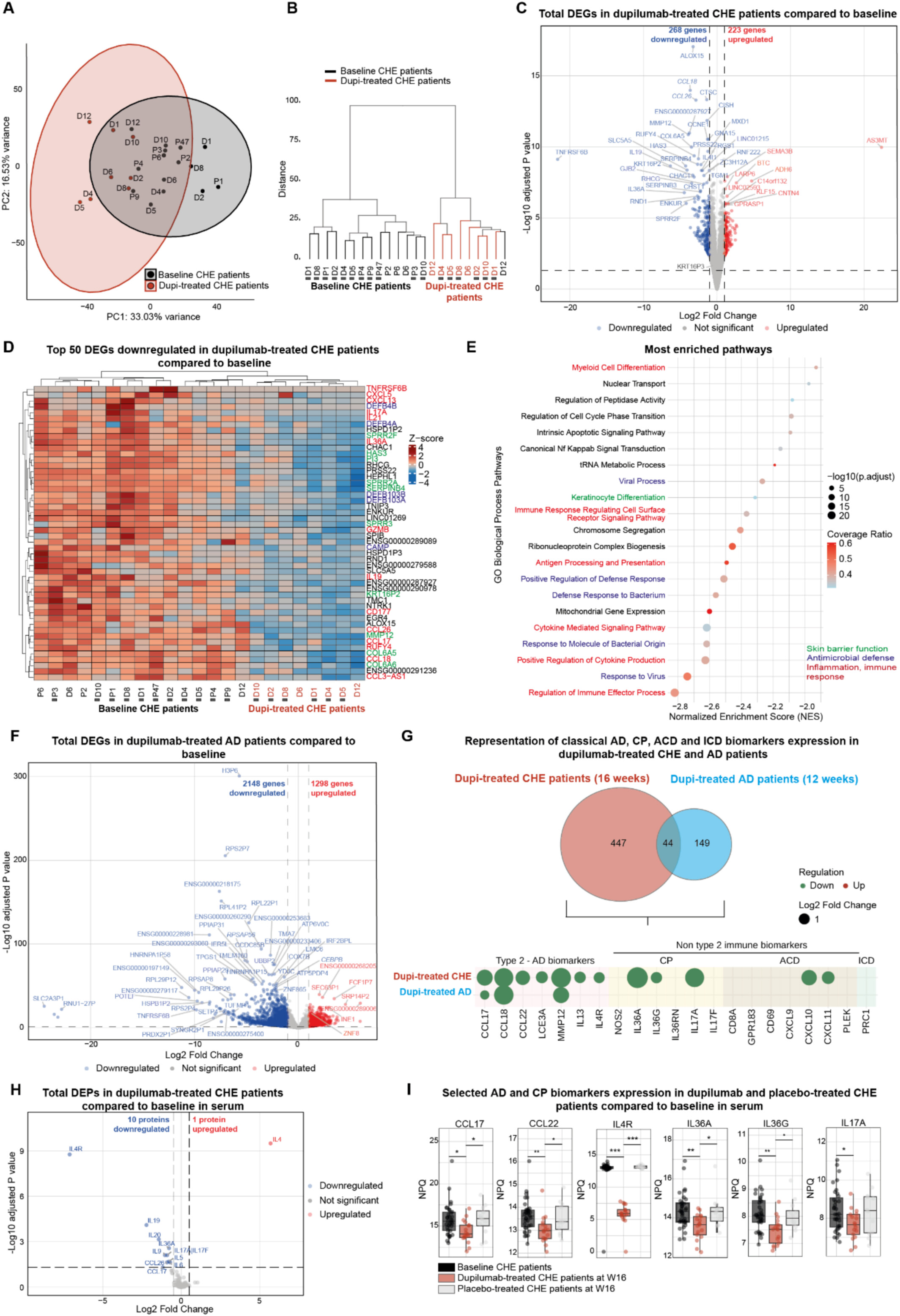
Fig. 4 度普利尤单抗修复CHE皮肤屏障并重建免疫稳态
文章总结
本研究明确了1、2、3型混合免疫紊乱伴皮肤屏障损伤是中重度CHE的核心分子病理特征,证实IL-4Rα信号是调控CHE病理特征与炎症签名的关键靶点。度普利尤单抗通过阻断IL-4Rα,可显著改善中重度CHE患者的临床症状,恢复皮肤屏障功能并重建免疫稳态,且疗效独立于AD病史、安全性良好,为无预筛选的中重度CHE患者提供了有效的广谱治疗策略,也为CHE的精准治疗与机制研究奠定了坚实的临床和分子基础。
原文链接:https://doi.org/10.1111/all.70263
研究背景
慢性手部湿疹(Chronic Hand Eczema, CHE)是常见的慢性炎症性皮肤病之一,其核心特征为疼痛、瘙痒及慢性炎症,病因复杂且受多种因素影响。该疾病临床表现多样,具有特应性皮炎(AD)、接触性皮炎及银屑病的重叠特征,这使得诊断与治疗工作极具挑战性。目前,慢性手部湿疹的潜在免疫机制尚未完全明确,仍需进一步深入研究。
2026年1月24日,法国里昂第一大学、图卢兹大学、波尔多大学等多机构联合团队在Allergy上发表了题为“Integrated Clinical Trial and Molecular Profiling Reveals Immune Drivers of Chronic Hand Eczema”的研究论文。该研究纳入94例中重度CHE患者,开展2b期随机双盲安慰剂对照临床试验,按1:1分为度普利尤单抗组与安慰剂组,整合皮肤转录组、血清和皮肤蛋白质组及光谱流式细胞术等多组学数据,系统探究了CHE的混合免疫驱动机制及IL-4Rα阻断治疗的疗效,为CHE的个体化治疗选择提供了关键参考。

文章标题
实验设计
样本队列:94例对强效外用糖皮质激素治疗无效、病程≥6个月的中重度CHE患者,按1:1随机分为度普利尤单抗治疗组(n=47)与安慰剂对照组(n=47),开展16周临床试验。
技术方法:整合了皮肤转录组学、皮肤和血清蛋白质组学及光谱流式细胞术,从基因、蛋白及免疫细胞表型多层面,系统刻画皮肤屏障功能与免疫炎症状态。

图形摘要
研究结果
01. CHE患者基线临床特征:异质性高,疾病负担显著
研究首先表明,特应性背景与临床表型是反映中重度CHE患者疾病负担的核心特征:有AD病史者更易合并过敏性鼻炎、哮喘等特应性疾病,且血清总IgE水平更高;临床表型以皲裂、角化过度为主,多表型叠加特征显著,76.6%患者双侧掌背同时受累。患者疾病平均病程8.72年,疾病负担随病程呈累积效应,基线mTLSS(改良皮损症状总评分)、DLQI(皮肤病生活质量指数)等指标显示其症状严重且生活质量受损显著,该特征在整合人口学、职业暴露等混杂因素后仍具稳定性(Fig. 1A),证实基线特征对CHE疾病评估具有独立参考价值。

Fig. 1 CHE患者基线临床特征
02. 度普利尤单抗治疗CHE疗效显著,且独立于AD背景
接下来,研究证实度普利尤单抗对中重度CHE的临床疗效显著优于安慰剂,且疗效独立于AD病史,为CHE广谱治疗提供关键证据。治疗16周后,度普利尤单抗组mTLSS平均改善59.8%,IGA、PaGA达清除或基本清除比例均超50%(Fig. 2A-D),患者瘙痒、疼痛等VAS评分及DLQI均显著改善(Fig. 2E-J),手部外湿疹症状也获缓解(Fig. 2L),且疗效经敏感性分析验证稳定;PCA分析显示,治疗干预是临床评分差异的关键因素,两组实现明显临床分层(Fig. 2K)。安全性上,两组不良事件发生率无显著差异,度普利尤单抗组以轻中度眼部不良事件为主,无严重不良事件致治疗中断,证实其用药安全性良好(Fig. 2L)。

Fig. 2 度普利尤单抗治疗CHE疗效显著,且独立于AD背景
03. CHE的核心分子病理特征:混合免疫紊乱伴皮肤屏障损伤
研究证实,中重度CHE患者的皮肤转录组、血清蛋白质组特征与AD、银屑病高度重叠,存在1、2、3型混合免疫紊乱,同时伴随皮肤屏障功能相关基因和蛋白的异常调控。皮肤转录组显示,CHE患者与健康对照相比存在3552个下调、1913个上调差异表达基因(Fig. 3A-C),富集于角质形成细胞分化、白细胞介导的免疫和细胞因子信号传导等通路,高表达AD相关2型、银屑病相关3型及少量1型免疫标志物,其差异基因与AD、经典银屑病的重叠比例分别达34.1%-52%、36.4%-39%(Fig. 3F-G);血清蛋白质组分析显示,其2、3型免疫相关蛋白显著上调,与皮肤转录组特征一致(Fig. 3H-J)。另外,CHE患者循环B细胞数量增多、NK细胞、Th2及Th17细胞减少,皮肤免疫细胞浸润分析显示活化记忆CD4⁺T细胞、树突状细胞富集,同时皮肤屏障相关基因和蛋白表达异常,证实其皮肤屏障功能严重受损。

Fig. 3 CHE的核心分子病理特征:混合免疫紊乱伴皮肤屏障损伤
04. 度普利尤单抗的作用机制:修复皮肤屏障,重建免疫稳态
最后,研究证实度普利尤单抗通过阻断IL-4Rα信号,不仅抑制2型免疫通路,还可调节1、3型免疫反应,进而逆转CHE患者分子层面异常,恢复皮肤屏障功能并重建免疫稳态。皮肤转录组分析显示,治疗后出现491个差异表达基因,2/3为下调基因,涵盖1、2、3型免疫及组织重塑、应激角蛋白相关基因,疾病相关通路被显著抑制(Fig. 4A-E);与AD患者治疗转录组对比,二者共享44个以2型免疫、屏障相关基因为主的核心差异基因,CHE还存在特异性1、3型免疫调控基因(Fig. 4F-G)。蛋白质组分析表明,治疗后皮肤屏障相关蛋白表达恢复正常,血清中2、3型免疫相关蛋白显著下调,仅IL4因受体阻断特异性上调(Fig. 4H);皮肤免疫细胞组成推断分析显示活化树突状细胞、记忆CD4⁺T细胞浸润减少,而安慰剂组无上述分子修复效应(Fig. 4I)。

Fig. 4 度普利尤单抗修复CHE皮肤屏障并重建免疫稳态
文章总结
本研究明确了1、2、3型混合免疫紊乱伴皮肤屏障损伤是中重度CHE的核心分子病理特征,证实IL-4Rα信号是调控CHE病理特征与炎症签名的关键靶点。度普利尤单抗通过阻断IL-4Rα,可显著改善中重度CHE患者的临床症状,恢复皮肤屏障功能并重建免疫稳态,且疗效独立于AD病史、安全性良好,为无预筛选的中重度CHE患者提供了有效的广谱治疗策略,也为CHE的精准治疗与机制研究奠定了坚实的临床和分子基础。
原文链接:https://doi.org/10.1111/all.70263







