研究背景
多发性硬化症(multiple sclerosis, MS)是一种以中枢神经系统炎性脱髓鞘和神经变性为特征的慢性自身免疫性疾病。当前 MS 的诊断主要依赖临床、影像学和脑脊液(CSF)分析(如寡克隆带,OCB)。然而,MS 的误诊和漏诊率仍居高不下(分别约影响七分之一和三分之一的MS患者),正确诊断往往需耗时一年以上。这种诊断延迟可能导致疾病修饰治疗(disease-modifying therapy,DMT)的启动延误或不必要使用。因此,亟需新的生物标志物来预测 MS 的长期进展及病程演变,从而更好地指导个体化治疗决策。
2026 年 2 月 25 日,马克斯普朗克生物化学研究所、慕尼黑工业大学等机构联合团队(Matthias Mann 为主要通讯联系人)在 Cell 发表题为“Large-scale proteomics across neurological disorders uncovers biomarker panel and targets in multiple sclerosis”的研究论文。该研究开展了迄今规模最大的脑脊液(CSF)蛋白质组学分析,不仅系统识别了影响CSF蛋白质组分析的关键混杂因素,更重要的是构建了一个由22个蛋白组成的诊断模型,能够显著提升 OCB 阴性多发性硬化症(MS)患者的诊断准确性。此外,研究还展示了 CSF 蛋白质组在预测 MS 疾病进展方面的巨大潜力,为推动 MS 向更精准的诊断、预后评估及治疗决策迈进提供了重要工具和新的研究见解。

文章标题
研究设计
队列样本:研究纳入一个大型横断面发现队列(5,045名不同捐赠者的CSF样本),涵盖MS、其他自身免疫性疾病、神经退行性疾病、感染、肿瘤、卒中以及神经科对照组等多种疾病。
组学检测:
首先使用timsTOF Pro 2对超过5,000份CSF样本进行了DIA分析,平均每个样本量化约1,500种蛋白质。
在研究后期,采用了更先进的Orbitrap Astral,对部分重点样本(约2,600份)进行了重新测量,每个样本蛋白质检测数量提升至约2,100种。
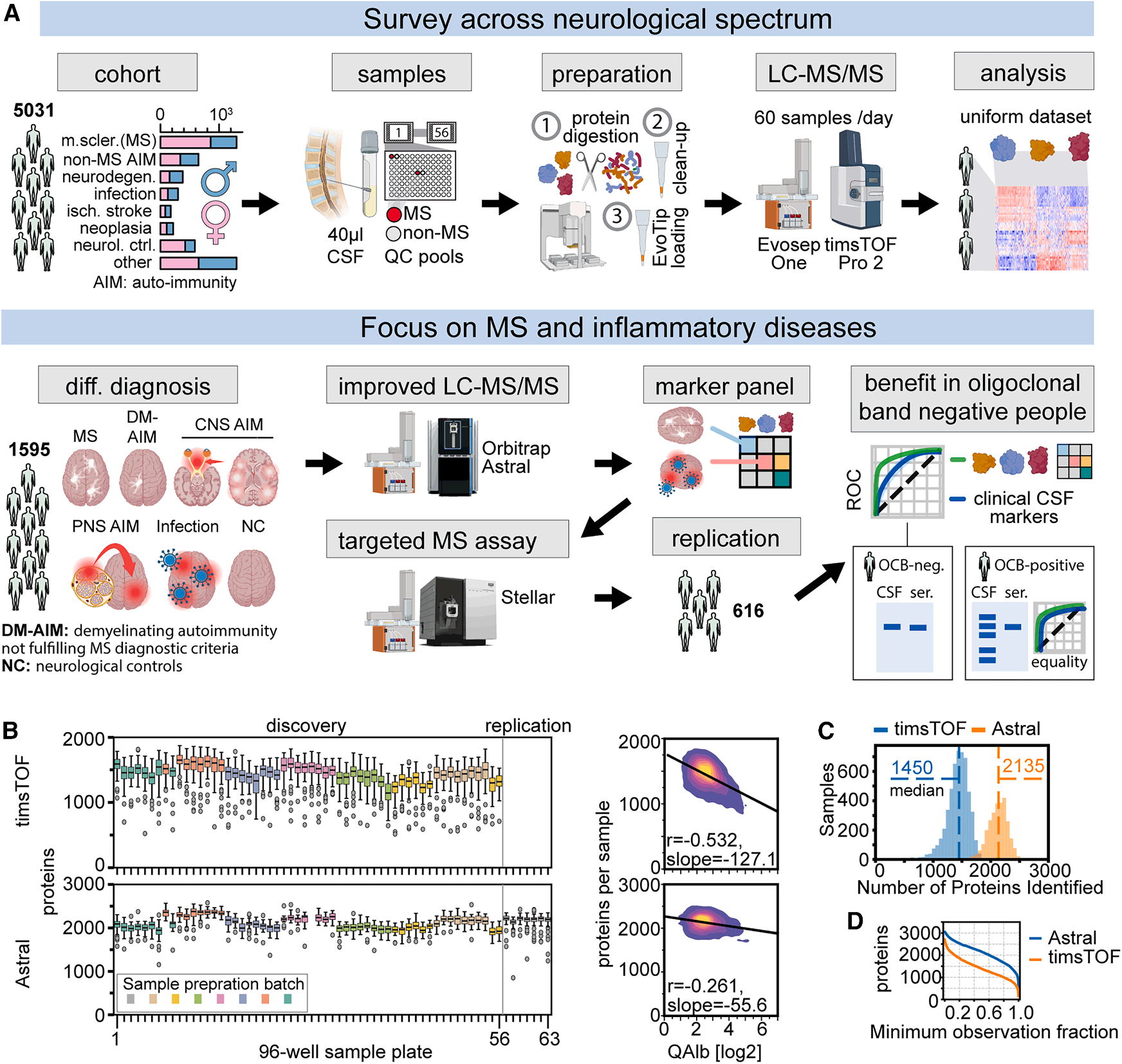
Fig. 1 研究概述
研究结果
01. 血液-脑脊液屏障损伤主导CSF蛋白质组变异
分析显示,BCB损伤(通过白蛋白比率QAlb衡量)是CSF蛋白质组最大的变异来源,其解释的变异量是临床诊断或其他协变量(如年龄、性别)的三倍。由于BCB损伤会导致大量血浆蛋白渗入CSF,若不校正,会掩盖真正的疾病信号。研究证明,在差异表达分析中必须将QAlb作为线性回归的协变量进行校正。同时研究发现血浆蛋白ITIH1或C5的CSF丰度与BCB损伤高度相关,可作为QAlb的替代指标,用于缺乏QAlb数据的研究。年龄、性别和CSF白细胞计数等协变量也解释了显著的蛋白质组变异,并调节了数百至数千种蛋白质。这些协变量的效应大多彼此独立,且与特定疾病的相互作用很小,因此在多变量模型中纳入这些协变量进行校正是有效的(Fig. 2)。
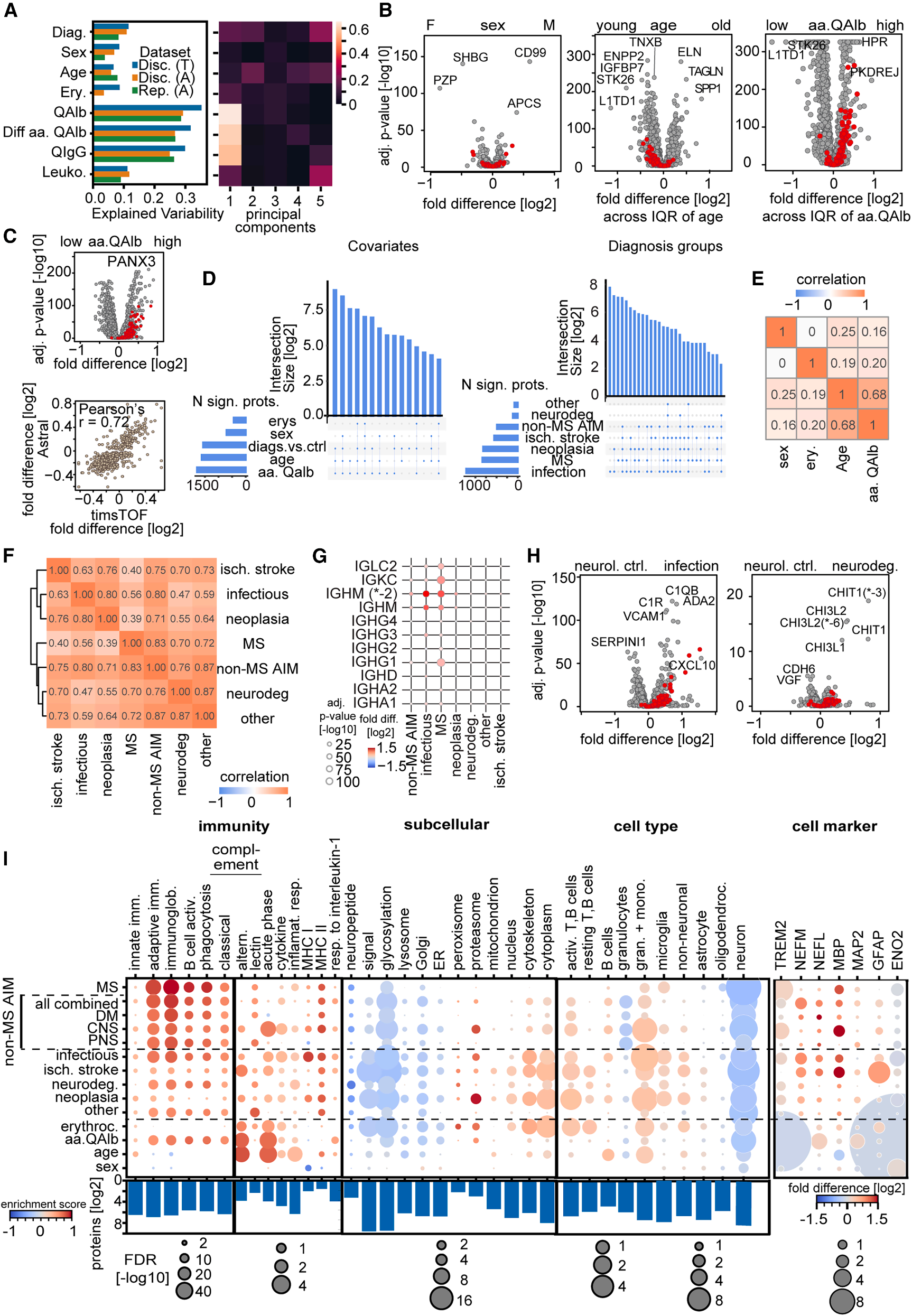
Fig. 2 诊断和协变量对脑脊液蛋白质组的影响
02. 多发性硬化症相关的脑脊液蛋白质组变化
通过对多发性硬化症(MS)、神经系统对照组以及其他自身免疫性疾病患者的脑脊液蛋白质组进行对比分析,研究人员发现在MS与所有其他神经系统疾病对比中,共有约77种蛋白质存在显著差异,其中约四分之三为免疫球蛋白,且以IgG亚型为主(Fig. 3C)。这凸显了B细胞及体液免疫在MS病理中的核心作用。相比之下,IgM蛋白则在感染性疾病中呈现更高的丰度。此外,约20种非免疫球蛋白蛋白质也与MS显著相关(Fig. 3E)。其中包括RYR2、CSF1R、CTSW等具有潜在治疗价值的蛋白质,以及参与髓鞘脂质代谢的ARSA和细胞外基质重塑相关蛋白RECK。这些分子为了解MS的发病机制提供了新的线索。同时上述蛋白质组的改变在使用蛋白质组学技术进行的对比分析中得到了验证,两种技术检测到的重叠且显著变化的蛋白质,其表达变化趋势高度一致,证实了结果的可靠性。
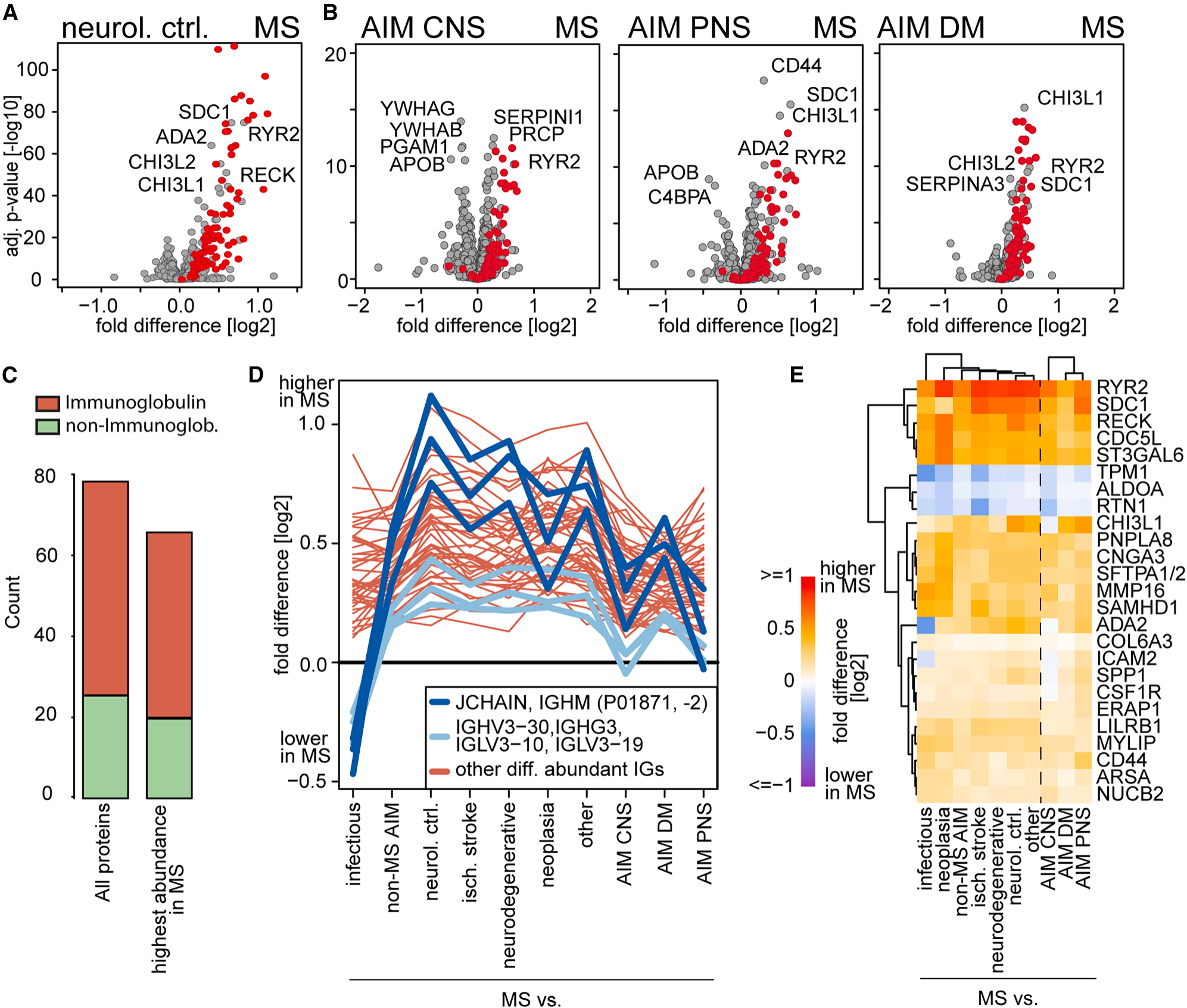
Fig. 3 多发性硬化症相关的脑脊液蛋白质组变化
03. 蛋白质组数据的多分类分析
本研究采用XGBoost算法对脑脊液蛋白质组数据进行多分类分析,机器学习模型在区分大多数神经系统疾病时表现良好,受试者AUC值介于0.80至0.91之间。然而,在区分多发性硬化症(MS)与其他脱髓鞘性自身免疫性疾病时,模型性能下降(AUC值 降至 0.76)(Fig. 4A-B),这反映了此类疾病在蛋白质组层面的相似性,也与临床实际诊断的难点相符。
前250个信息最丰富的蛋白质贡献了约70%的模型判别信息,其中MBP、CHIT1、CTSW等是区分MS的关键蛋白质。在通路层面,适应性免疫相关特征对MS具有正向预测价值,而固有免疫相关特征则相反(Fig. 4H)。此外,年龄和脑脊液白细胞计数是较强的疾病鉴别协变量,而血脑屏障损伤的影响主要体现在模型的第二个主成分上。
基于蛋白质组数据构建的“拟时序”疾病轨迹显示:神经系统对照组聚集在拟时序轴的早期,而MS患者则分布于晚期。该拟时序分期与患者采样时的临床残疾评分(ARMSS)显著相关,表明分子分期能够反映疾病的严重程度。随着拟时序评分升高,免疫球蛋白、MBP、神经丝蛋白等与神经炎症和轴索损伤相关的蛋白质丰度也呈现上升趋势(Fig. 4I-J)。
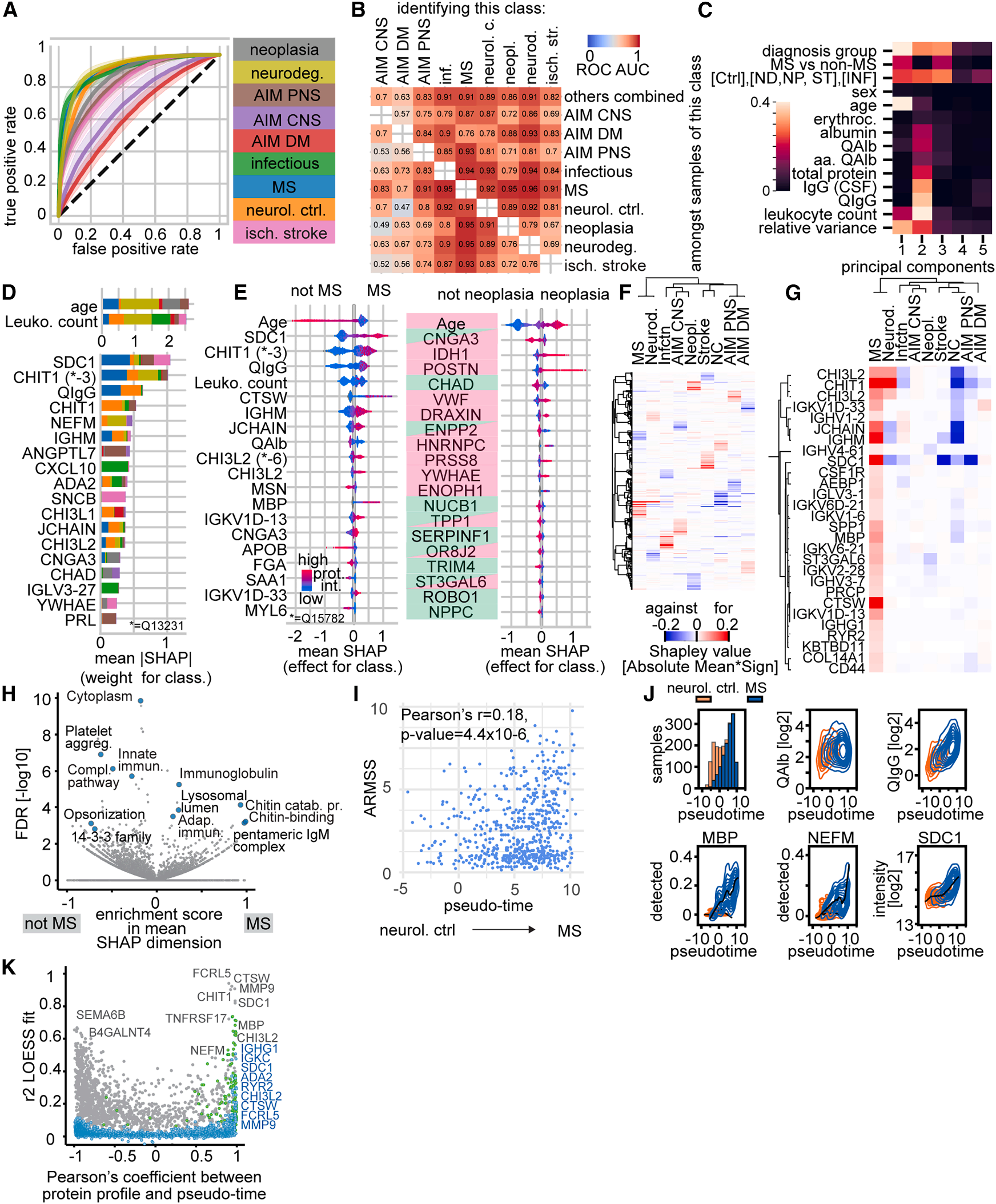
Fig. 4 多分类分析比较
04. 构建用于多发性硬化症(MS)诊断的蛋白质组学生物标志物模型
为构建并验证用于多发性硬化症(MS)诊断的蛋白质组学生物标志物模型,从总队列中,按年龄、性别及OCB状态等关键协变量进行分层,选取了包含MS、其他炎症性疾病及对照组的1600份样本,并使用高分辨质谱(Orbitrap Astral)进行了深度蛋白质组学分析(Fig. 5A),确保了数据的质量与覆盖度(>2000种蛋白)。
以所有量化蛋白及年龄、性别为特征,通过机器学习筛选出一个包含30个特征(主要为蛋白质)的诊断模型。在所有样本中,该蛋白质组学模型的诊断性能与现有临床标志物组合(包括OCB状态、IgG比率、白蛋白比率等)相当(Fig. 5C-E)。在该临床诊断的难点人群里,该模型用于区分MS与中枢神经系统/周围神经系统自身免疫性疾病的效能显著优于临床参考模型,AUC值提升约0.1-0.2。这一优势在一个包含600份样本的独立验证队列中得到了确认(Fig. 5E)。
该标志物模型涵盖了MS多个关键病理过程的代表性蛋白,例如:MBP(髓鞘碱性蛋白):反映髓鞘破坏。NEFM(神经丝中分子):指示轴索损伤。C1QB(补体C1q亚基):提示小胶质细胞/固有免疫激活。模型通过整合这些互补的生物学信息,实现了对MS,特别是OCB阴性MS更精准的分子辨识。
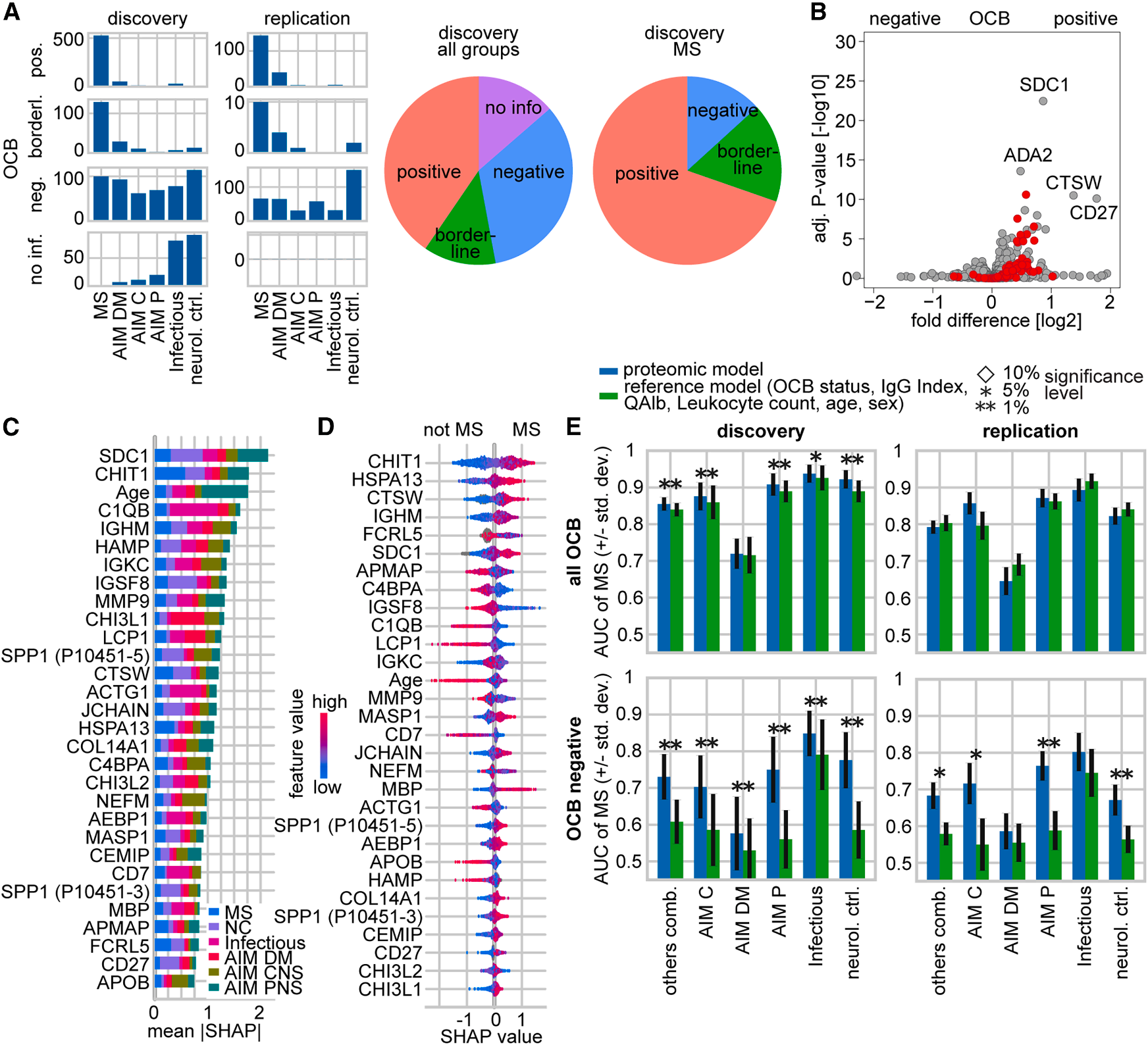
Fig. 5 用于OCB阳性和阴性多发性硬化症的生物标志物模型
05. 蛋白标志物模型的靶向检测方法建立
为推进生物标志物的临床转化,研究人员基于前期发现的蛋白质标志物,在Thermo Fisher Stellar质谱仪上构建了一个靶向检测方法(Fig. 6A-D)。通过对29种候选蛋白的分析,最终依据信号质量与流程稳定性,筛选出22种蛋白质(每种蛋白定量1条特征肽段)构成最终检测模型。这些标志物的生物学效应强度远高于检测流程本身的变异(通常是流程变异的5-15倍)。使用该靶向方法进行定量分析后,蛋白质组学模型的诊断性能得到进一步巩固和提升。在所有样本(无论OCB状态)以及关键的OCB阴性样本中,其诊断效能均持续优于临床参考模型。相较于临床模型,其AUC值提升了0.02至0.1(Fig. 6E)。而且该靶向检测方法展现出良好的稳健性。即使在脑脊液上样量减少30%甚至60%的挑战性条件下,其检测性能和诊断能力也未受到显著影响,表明该方法适用于实际临床实验室中可能遇到的样本量波动情况(Fig. 6F)。
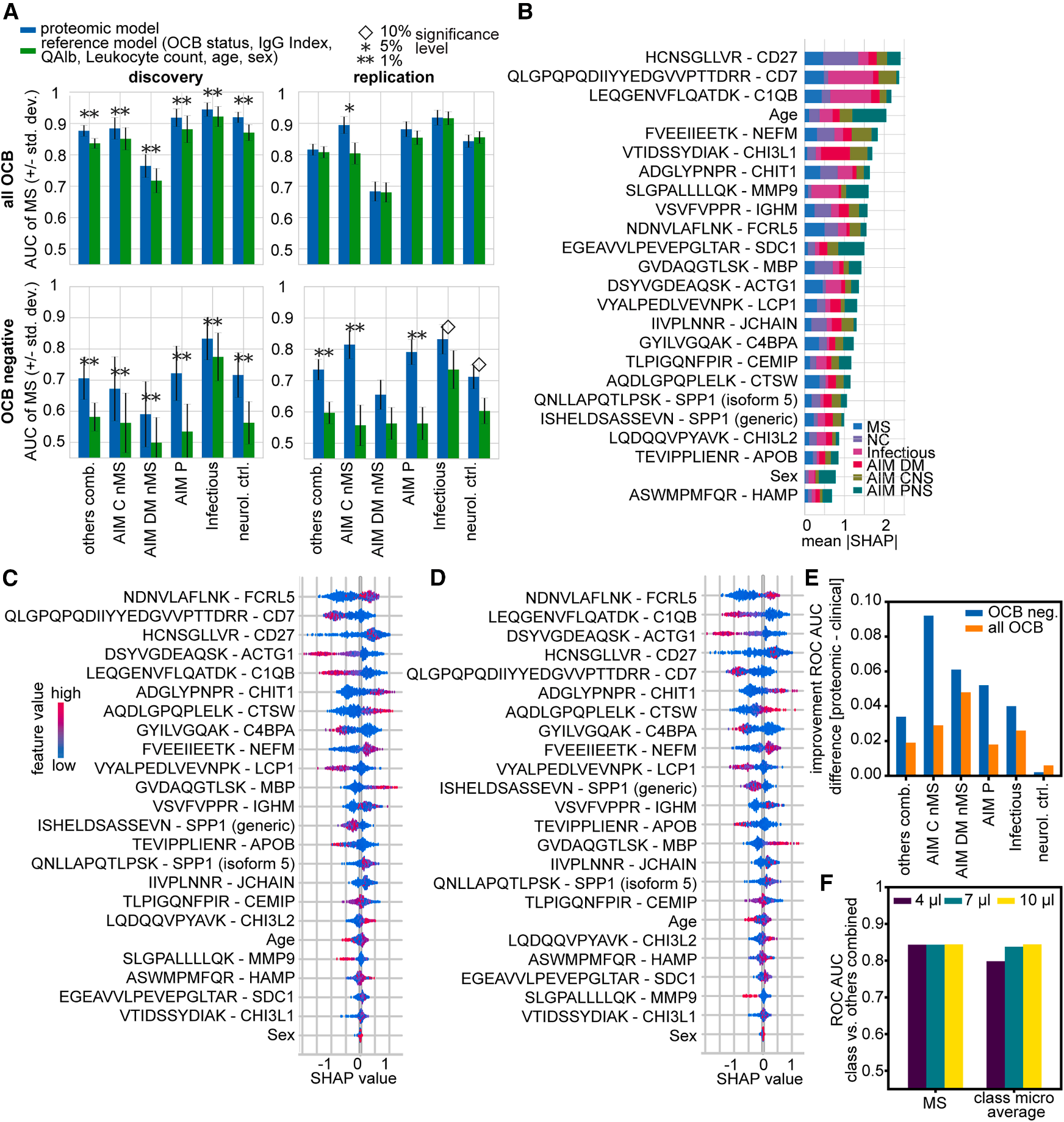
Fig. 6 22 种蛋白质模型的靶向检测
06. 复发缓解型(RRMS)与进展型(PMS)患者的脑脊液蛋白质组对比分析
通过对复发缓解型多发性硬化症(RRMS)与进展型多发性硬化症(PMS,包括PPMS和SPMS)患者的脑脊液蛋白质组进行对比分析,研究人员发现原发性进展型(PPMS)与继发性进展型(SPMS)患者表现出高度相似的蛋白质组改变,这与它们同属进展型病程的临床特征一致(Fig. 7A-C)。而机器学习鉴别分析揭示,适应性免疫相关标志物更多地指向RRMS,而固有免疫特征(如补体激活)则在PMS中占主导(Fig. 7D-E)。此外,与神经胶质细胞耗竭相关的SERPINA3及转化生长因子-β信号通路成分TGFBR1也与PMS显著相关。
蛋白质组“拟时序”分析显示,RRMS与PMS患者在疾病连续谱上呈连续分布,且该拟时序分期与患者当时的残疾程度(ARMSS评分)显著相关,这一关联在独立验证队列中得到确认。更具预后价值的是,在基线处于RRMS的患者中,那些后来转化为SPMS的患者,其基线“拟时序”评分显著高于未转化者。此外,更高的“拟时序”评分与更短的转化时间间隔相关。这表明,基于脑脊液蛋白质组的分子分期,能够在疾病早期有效预测RRMS向SPMS的病程转化风险。
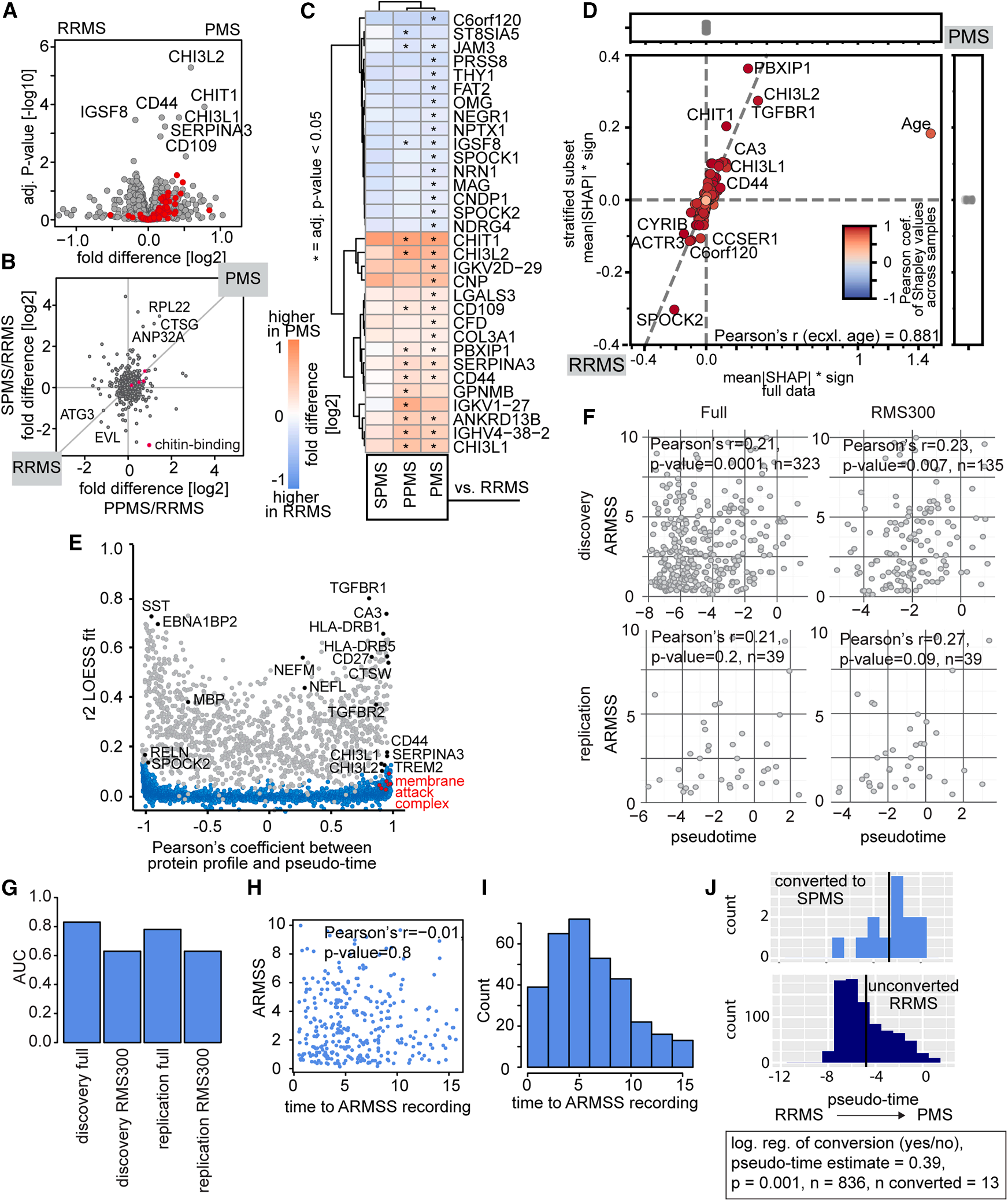
Fig. 7 复发缓解型和进展型多发性硬化症的脑脊液变化及疾病病程转化
总结与展望
本研究通过对大规模脑脊液蛋白质组进行系统性分析,揭示了神经系统疾病相关的分子图谱,并首次量化了血脑屏障损伤是影响蛋白质组数据的首要混杂因素,年龄与性别也是重要的协变量。基于此,该研究团队开发了一个包含22种蛋白质的生物标志物模型,其在多发性硬化症(MS)的鉴别诊断中展现出卓越性能,尤其在临床诊断难点——OCB阴性患者中,诊断效能显著优于现有临床标志物组合,且适用于所有OCB状态的患者。该模型已成功转化为一项基于靶向质谱的稳健、可推广的检测方法。
此外,本研究提出的蛋白质组“拟时序”分期与MS患者的即时残疾程度、疾病进展阶段密切相关,并能有效预测复发缓解型MS向继发进展型MS转化的风险,为疾病进展评估提供了新的分子工具。这项工作不仅为MS的精准诊断、预后预测及治疗靶点发现提供了切实可行的解决方案,也为未来大规模脑脊液蛋白质组学研究在神经疾病领域的应用,建立了重要的技术流程与分析范式。
原文链接:https://www.cell.com/cell/fulltext/S0092-8674(26)00104-2?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867426001042%3Fshowall%3Dtrue
研究背景
多发性硬化症(multiple sclerosis, MS)是一种以中枢神经系统炎性脱髓鞘和神经变性为特征的慢性自身免疫性疾病。当前 MS 的诊断主要依赖临床、影像学和脑脊液(CSF)分析(如寡克隆带,OCB)。然而,MS 的误诊和漏诊率仍居高不下(分别约影响七分之一和三分之一的MS患者),正确诊断往往需耗时一年以上。这种诊断延迟可能导致疾病修饰治疗(disease-modifying therapy,DMT)的启动延误或不必要使用。因此,亟需新的生物标志物来预测 MS 的长期进展及病程演变,从而更好地指导个体化治疗决策。
2026 年 2 月 25 日,马克斯普朗克生物化学研究所、慕尼黑工业大学等机构联合团队(Matthias Mann 为主要通讯联系人)在 Cell 发表题为“Large-scale proteomics across neurological disorders uncovers biomarker panel and targets in multiple sclerosis”的研究论文。该研究开展了迄今规模最大的脑脊液(CSF)蛋白质组学分析,不仅系统识别了影响CSF蛋白质组分析的关键混杂因素,更重要的是构建了一个由22个蛋白组成的诊断模型,能够显著提升 OCB 阴性多发性硬化症(MS)患者的诊断准确性。此外,研究还展示了 CSF 蛋白质组在预测 MS 疾病进展方面的巨大潜力,为推动 MS 向更精准的诊断、预后评估及治疗决策迈进提供了重要工具和新的研究见解。

文章标题
研究设计
队列样本:研究纳入一个大型横断面发现队列(5,045名不同捐赠者的CSF样本),涵盖MS、其他自身免疫性疾病、神经退行性疾病、感染、肿瘤、卒中以及神经科对照组等多种疾病。
组学检测:
首先使用timsTOF Pro 2对超过5,000份CSF样本进行了DIA分析,平均每个样本量化约1,500种蛋白质。
在研究后期,采用了更先进的Orbitrap Astral,对部分重点样本(约2,600份)进行了重新测量,每个样本蛋白质检测数量提升至约2,100种。

Fig. 1 研究概述
研究结果
01. 血液-脑脊液屏障损伤主导CSF蛋白质组变异
分析显示,BCB损伤(通过白蛋白比率QAlb衡量)是CSF蛋白质组最大的变异来源,其解释的变异量是临床诊断或其他协变量(如年龄、性别)的三倍。由于BCB损伤会导致大量血浆蛋白渗入CSF,若不校正,会掩盖真正的疾病信号。研究证明,在差异表达分析中必须将QAlb作为线性回归的协变量进行校正。同时研究发现血浆蛋白ITIH1或C5的CSF丰度与BCB损伤高度相关,可作为QAlb的替代指标,用于缺乏QAlb数据的研究。年龄、性别和CSF白细胞计数等协变量也解释了显著的蛋白质组变异,并调节了数百至数千种蛋白质。这些协变量的效应大多彼此独立,且与特定疾病的相互作用很小,因此在多变量模型中纳入这些协变量进行校正是有效的(Fig. 2)。

Fig. 2 诊断和协变量对脑脊液蛋白质组的影响
02. 多发性硬化症相关的脑脊液蛋白质组变化
通过对多发性硬化症(MS)、神经系统对照组以及其他自身免疫性疾病患者的脑脊液蛋白质组进行对比分析,研究人员发现在MS与所有其他神经系统疾病对比中,共有约77种蛋白质存在显著差异,其中约四分之三为免疫球蛋白,且以IgG亚型为主(Fig. 3C)。这凸显了B细胞及体液免疫在MS病理中的核心作用。相比之下,IgM蛋白则在感染性疾病中呈现更高的丰度。此外,约20种非免疫球蛋白蛋白质也与MS显著相关(Fig. 3E)。其中包括RYR2、CSF1R、CTSW等具有潜在治疗价值的蛋白质,以及参与髓鞘脂质代谢的ARSA和细胞外基质重塑相关蛋白RECK。这些分子为了解MS的发病机制提供了新的线索。同时上述蛋白质组的改变在使用蛋白质组学技术进行的对比分析中得到了验证,两种技术检测到的重叠且显著变化的蛋白质,其表达变化趋势高度一致,证实了结果的可靠性。

Fig. 3 多发性硬化症相关的脑脊液蛋白质组变化
03. 蛋白质组数据的多分类分析
本研究采用XGBoost算法对脑脊液蛋白质组数据进行多分类分析,机器学习模型在区分大多数神经系统疾病时表现良好,受试者AUC值介于0.80至0.91之间。然而,在区分多发性硬化症(MS)与其他脱髓鞘性自身免疫性疾病时,模型性能下降(AUC值 降至 0.76)(Fig. 4A-B),这反映了此类疾病在蛋白质组层面的相似性,也与临床实际诊断的难点相符。
前250个信息最丰富的蛋白质贡献了约70%的模型判别信息,其中MBP、CHIT1、CTSW等是区分MS的关键蛋白质。在通路层面,适应性免疫相关特征对MS具有正向预测价值,而固有免疫相关特征则相反(Fig. 4H)。此外,年龄和脑脊液白细胞计数是较强的疾病鉴别协变量,而血脑屏障损伤的影响主要体现在模型的第二个主成分上。
基于蛋白质组数据构建的“拟时序”疾病轨迹显示:神经系统对照组聚集在拟时序轴的早期,而MS患者则分布于晚期。该拟时序分期与患者采样时的临床残疾评分(ARMSS)显著相关,表明分子分期能够反映疾病的严重程度。随着拟时序评分升高,免疫球蛋白、MBP、神经丝蛋白等与神经炎症和轴索损伤相关的蛋白质丰度也呈现上升趋势(Fig. 4I-J)。

Fig. 4 多分类分析比较
04. 构建用于多发性硬化症(MS)诊断的蛋白质组学生物标志物模型
为构建并验证用于多发性硬化症(MS)诊断的蛋白质组学生物标志物模型,从总队列中,按年龄、性别及OCB状态等关键协变量进行分层,选取了包含MS、其他炎症性疾病及对照组的1600份样本,并使用高分辨质谱(Orbitrap Astral)进行了深度蛋白质组学分析(Fig. 5A),确保了数据的质量与覆盖度(>2000种蛋白)。
以所有量化蛋白及年龄、性别为特征,通过机器学习筛选出一个包含30个特征(主要为蛋白质)的诊断模型。在所有样本中,该蛋白质组学模型的诊断性能与现有临床标志物组合(包括OCB状态、IgG比率、白蛋白比率等)相当(Fig. 5C-E)。在该临床诊断的难点人群里,该模型用于区分MS与中枢神经系统/周围神经系统自身免疫性疾病的效能显著优于临床参考模型,AUC值提升约0.1-0.2。这一优势在一个包含600份样本的独立验证队列中得到了确认(Fig. 5E)。
该标志物模型涵盖了MS多个关键病理过程的代表性蛋白,例如:MBP(髓鞘碱性蛋白):反映髓鞘破坏。NEFM(神经丝中分子):指示轴索损伤。C1QB(补体C1q亚基):提示小胶质细胞/固有免疫激活。模型通过整合这些互补的生物学信息,实现了对MS,特别是OCB阴性MS更精准的分子辨识。

Fig. 5 用于OCB阳性和阴性多发性硬化症的生物标志物模型
05. 蛋白标志物模型的靶向检测方法建立
为推进生物标志物的临床转化,研究人员基于前期发现的蛋白质标志物,在Thermo Fisher Stellar质谱仪上构建了一个靶向检测方法(Fig. 6A-D)。通过对29种候选蛋白的分析,最终依据信号质量与流程稳定性,筛选出22种蛋白质(每种蛋白定量1条特征肽段)构成最终检测模型。这些标志物的生物学效应强度远高于检测流程本身的变异(通常是流程变异的5-15倍)。使用该靶向方法进行定量分析后,蛋白质组学模型的诊断性能得到进一步巩固和提升。在所有样本(无论OCB状态)以及关键的OCB阴性样本中,其诊断效能均持续优于临床参考模型。相较于临床模型,其AUC值提升了0.02至0.1(Fig. 6E)。而且该靶向检测方法展现出良好的稳健性。即使在脑脊液上样量减少30%甚至60%的挑战性条件下,其检测性能和诊断能力也未受到显著影响,表明该方法适用于实际临床实验室中可能遇到的样本量波动情况(Fig. 6F)。

Fig. 6 22 种蛋白质模型的靶向检测
06. 复发缓解型(RRMS)与进展型(PMS)患者的脑脊液蛋白质组对比分析
通过对复发缓解型多发性硬化症(RRMS)与进展型多发性硬化症(PMS,包括PPMS和SPMS)患者的脑脊液蛋白质组进行对比分析,研究人员发现原发性进展型(PPMS)与继发性进展型(SPMS)患者表现出高度相似的蛋白质组改变,这与它们同属进展型病程的临床特征一致(Fig. 7A-C)。而机器学习鉴别分析揭示,适应性免疫相关标志物更多地指向RRMS,而固有免疫特征(如补体激活)则在PMS中占主导(Fig. 7D-E)。此外,与神经胶质细胞耗竭相关的SERPINA3及转化生长因子-β信号通路成分TGFBR1也与PMS显著相关。
蛋白质组“拟时序”分析显示,RRMS与PMS患者在疾病连续谱上呈连续分布,且该拟时序分期与患者当时的残疾程度(ARMSS评分)显著相关,这一关联在独立验证队列中得到确认。更具预后价值的是,在基线处于RRMS的患者中,那些后来转化为SPMS的患者,其基线“拟时序”评分显著高于未转化者。此外,更高的“拟时序”评分与更短的转化时间间隔相关。这表明,基于脑脊液蛋白质组的分子分期,能够在疾病早期有效预测RRMS向SPMS的病程转化风险。

Fig. 7 复发缓解型和进展型多发性硬化症的脑脊液变化及疾病病程转化
总结与展望
本研究通过对大规模脑脊液蛋白质组进行系统性分析,揭示了神经系统疾病相关的分子图谱,并首次量化了血脑屏障损伤是影响蛋白质组数据的首要混杂因素,年龄与性别也是重要的协变量。基于此,该研究团队开发了一个包含22种蛋白质的生物标志物模型,其在多发性硬化症(MS)的鉴别诊断中展现出卓越性能,尤其在临床诊断难点——OCB阴性患者中,诊断效能显著优于现有临床标志物组合,且适用于所有OCB状态的患者。该模型已成功转化为一项基于靶向质谱的稳健、可推广的检测方法。
此外,本研究提出的蛋白质组“拟时序”分期与MS患者的即时残疾程度、疾病进展阶段密切相关,并能有效预测复发缓解型MS向继发进展型MS转化的风险,为疾病进展评估提供了新的分子工具。这项工作不仅为MS的精准诊断、预后预测及治疗靶点发现提供了切实可行的解决方案,也为未来大规模脑脊液蛋白质组学研究在神经疾病领域的应用,建立了重要的技术流程与分析范式。
原文链接:https://www.cell.com/cell/fulltext/S0092-8674(26)00104-2?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867426001042%3Fshowall%3Dtrue