研究背景
急性缺血性卒中(Acute Ischemic Stroke, AIS)是由于脑动脉发生急性阻塞,导致局部脑组织缺血缺氧并迅速发生坏死的一类脑血管疾病,是全球范围内导致死亡和致残的主要原因之一。其临床结局受多种因素影响,其中血栓的组成成分被认为是关键决定因素。组织病理学研究显示,血栓主要由红细胞、血小板、纤维蛋白及多种免疫细胞构成,其中中性粒细胞被视为动脉血栓形成的重要参与者。越来越多的研究证据表明,动脉血栓内中性粒细胞的浸润程度会随时间逐渐加重,这不仅削弱血运重建的治疗效果,还与不良临床结局密切相关。
2026年3月3日,暨南大学附属第一医院逯丹研究员/徐安定教授团队联合中山大学孙逸仙纪念医院麦鸿成副研究员在《Blood》期刊上发表了题为"Pathogenic Role of SERPINB3-positive Neutrophils in Reinforcing Thrombus Stiffening during Ischemic Stroke"的研究论文。本研究通过整合3D成像、多重免疫荧光染色和激光捕获显微切割空间蛋白质组学技术,系统性地揭示了中性粒细胞来源的SERPINB3通过TGFβ1-NET-COL1A1信号轴促进血栓硬化的分子机制,为AIS的预后生物标志物和治疗靶点开发提供了重要理论依据。西湖欧米为该研究提供了蛋白质组学检测服务。

文章标题
研究设计
本研究纳入队列包括56名AIS患者(发现队列34名+验证队列22名),采集机械取栓术后血栓样本开展空间蛋白质组学分析。
多组学技术包括:
◊3D组织透明化成像和多重免疫荧光染色用于绘制血栓免疫细胞空间分布图谱
◊激光捕获显微切割(LCM)空间蛋白质组学分离并鉴定血栓中性粒细胞蛋白质组特征
◊原子力显微镜(AFM)量化血栓纳米力学特性
◊单细胞蛋白质组学分析SERPINB3表达与患者预后的关联
验证方法:
◊外部验证队列(22例患者)验证SERPINB3作为预后标志物的可靠性
◊FeCl₃诱导颈动脉血栓模型和小鼠大脑中动脉闭塞(MCAO)模型
◊中性粒细胞耗竭实验和32Dcl3细胞来源的中性粒细胞移植实验
◊Serpinb3a基因敲除小鼠和siRNA knockdown实验验证SERPINB3功能
研究结果
01. 中性粒细胞是AIS血栓中主要的免疫细胞群体,与血栓硬度增加和不良预后相关
通过3D组织透明化成像和多重免疫荧光染色,研究者绘制了AIS患者血栓的免疫细胞空间分布图谱(Fig. 1A-C)。结果显示,中性粒细胞(MPO⁺)是最丰富的免疫细胞群体,其次是波形蛋白阳性成纤维细胞样细胞。3D成像显示Ly6G⁺中性粒细胞集中在血栓外周富含胶原蛋白的区域。Masson染色时间序列分析显示中性粒细胞富集区域与胶原蛋白沉积随时间增加(Fig. 1D, 1E)。MPO与TGFβ1、FSP1的共定位分析进一步证实了这种空间关联(Fig. 1F, 1G)。COL1A1⁺/MPO⁺细胞比例和AFM测量的硬度(Fig. 1H-K)均与90天改良Rankin量表(mRS)评分呈强正相关(Spearman R=0.634, p<0.001),提示中性粒细胞相关的胶原蛋白沉积和血栓硬度是AIS长期功能不良结局的关键驱动因素。

图1:患者血栓中中性粒细胞的分布及其与血栓硬度的相关性

图2:中性粒细胞对血栓形成和僵硬的影响
03. 空间蛋白质组学鉴定SERPINB3为AIS血栓预后标志物

图3:血栓中性粒细胞的空间蛋白质组学分析
04. 中性粒细胞来源的SERPINB3促进动脉血栓硬化并损害卒中恢复
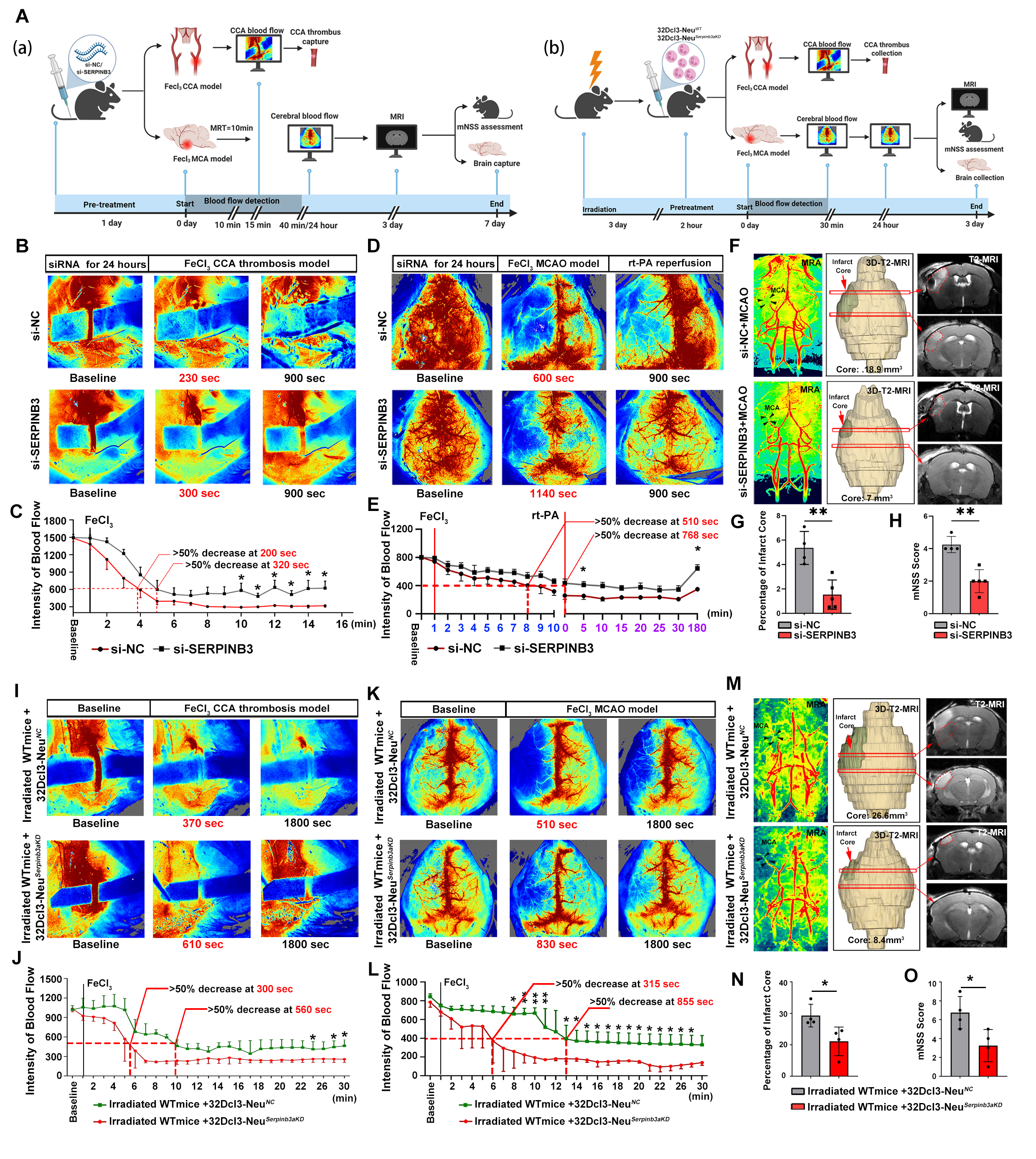
图4:中性粒细胞来源的SERPINB3对小鼠血栓形成和预后的影响
05. 中性粒细胞SERPINB3-TGFβ1轴促进胶原蛋白沉积和血栓硬化

图5:Serpinb3a缺陷和受照射小鼠血栓形成、僵硬和脑灌注的评估
在细胞水平,TBHP刺激诱导HL-60细胞中SERPINB3、TGFβ1、CitH3和COL1A1时间依赖性上调(Fig. 6A, 6D)。NET降解实验显示DNase I降低CitH3但不影响SERPINB3,提示SERPINB3作用于NET上游(Fig. 6B, 6E)。重组SERPINB3处理上调COL1A1、TGFβ1、CitH3,而这些效应可被Metelimumab逆转(Fig. 6C, 6F)。AFM和免疫荧光证实rSERPINB3增加血栓硬度和COL1A1沉积,TGFβ1抑制可逆转(Fig. 6G-I)。这些数据共同证明中性粒细胞SERPINB3-TGFβ1-NET-胶原蛋白信号轴通过ROS响应机制增强血栓形成并促进血栓硬化(Fig. 6J)。
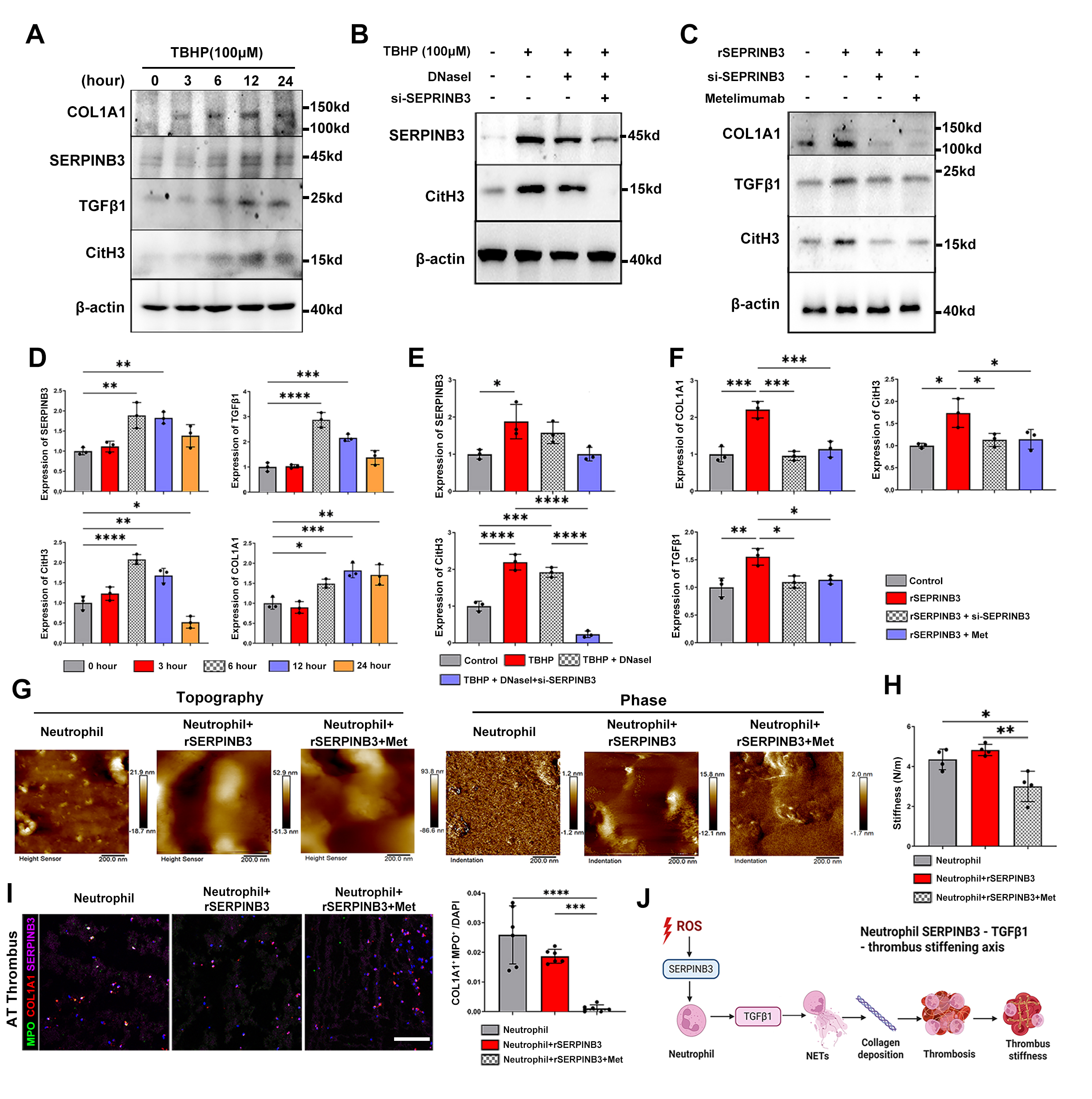
图6:中性粒细胞中SERPINB3的表达通过TGFβ1介导的胶原沉积促进血栓硬化
原文链接:https://doi.org/10.1182/blood.2025029516
研究背景
急性缺血性卒中(Acute Ischemic Stroke, AIS)是由于脑动脉发生急性阻塞,导致局部脑组织缺血缺氧并迅速发生坏死的一类脑血管疾病,是全球范围内导致死亡和致残的主要原因之一。其临床结局受多种因素影响,其中血栓的组成成分被认为是关键决定因素。组织病理学研究显示,血栓主要由红细胞、血小板、纤维蛋白及多种免疫细胞构成,其中中性粒细胞被视为动脉血栓形成的重要参与者。越来越多的研究证据表明,动脉血栓内中性粒细胞的浸润程度会随时间逐渐加重,这不仅削弱血运重建的治疗效果,还与不良临床结局密切相关。
2026年3月3日,暨南大学附属第一医院逯丹研究员/徐安定教授团队联合中山大学孙逸仙纪念医院麦鸿成副研究员在《Blood》期刊上发表了题为"Pathogenic Role of SERPINB3-positive Neutrophils in Reinforcing Thrombus Stiffening during Ischemic Stroke"的研究论文。本研究通过整合3D成像、多重免疫荧光染色和激光捕获显微切割空间蛋白质组学技术,系统性地揭示了中性粒细胞来源的SERPINB3通过TGFβ1-NET-COL1A1信号轴促进血栓硬化的分子机制,为AIS的预后生物标志物和治疗靶点开发提供了重要理论依据。西湖欧米为该研究提供了蛋白质组学检测服务。

文章标题
研究设计
本研究纳入队列包括56名AIS患者(发现队列34名+验证队列22名),采集机械取栓术后血栓样本开展空间蛋白质组学分析。
多组学技术包括:
◊3D组织透明化成像和多重免疫荧光染色用于绘制血栓免疫细胞空间分布图谱
◊激光捕获显微切割(LCM)空间蛋白质组学分离并鉴定血栓中性粒细胞蛋白质组特征
◊原子力显微镜(AFM)量化血栓纳米力学特性
◊单细胞蛋白质组学分析SERPINB3表达与患者预后的关联
验证方法:
◊外部验证队列(22例患者)验证SERPINB3作为预后标志物的可靠性
◊FeCl₃诱导颈动脉血栓模型和小鼠大脑中动脉闭塞(MCAO)模型
◊中性粒细胞耗竭实验和32Dcl3细胞来源的中性粒细胞移植实验
◊Serpinb3a基因敲除小鼠和siRNA knockdown实验验证SERPINB3功能
研究结果
01. 中性粒细胞是AIS血栓中主要的免疫细胞群体,与血栓硬度增加和不良预后相关
通过3D组织透明化成像和多重免疫荧光染色,研究者绘制了AIS患者血栓的免疫细胞空间分布图谱(Fig. 1A-C)。结果显示,中性粒细胞(MPO⁺)是最丰富的免疫细胞群体,其次是波形蛋白阳性成纤维细胞样细胞。3D成像显示Ly6G⁺中性粒细胞集中在血栓外周富含胶原蛋白的区域。Masson染色时间序列分析显示中性粒细胞富集区域与胶原蛋白沉积随时间增加(Fig. 1D, 1E)。MPO与TGFβ1、FSP1的共定位分析进一步证实了这种空间关联(Fig. 1F, 1G)。COL1A1⁺/MPO⁺细胞比例和AFM测量的硬度(Fig. 1H-K)均与90天改良Rankin量表(mRS)评分呈强正相关(Spearman R=0.634, p<0.001),提示中性粒细胞相关的胶原蛋白沉积和血栓硬度是AIS长期功能不良结局的关键驱动因素。

图1:患者血栓中中性粒细胞的分布及其与血栓硬度的相关性

图2:中性粒细胞对血栓形成和僵硬的影响
03. 空间蛋白质组学鉴定SERPINB3为AIS血栓预后标志物

图3:血栓中性粒细胞的空间蛋白质组学分析
04. 中性粒细胞来源的SERPINB3促进动脉血栓硬化并损害卒中恢复

图4:中性粒细胞来源的SERPINB3对小鼠血栓形成和预后的影响
05. 中性粒细胞SERPINB3-TGFβ1轴促进胶原蛋白沉积和血栓硬化

图5:Serpinb3a缺陷和受照射小鼠血栓形成、僵硬和脑灌注的评估
在细胞水平,TBHP刺激诱导HL-60细胞中SERPINB3、TGFβ1、CitH3和COL1A1时间依赖性上调(Fig. 6A, 6D)。NET降解实验显示DNase I降低CitH3但不影响SERPINB3,提示SERPINB3作用于NET上游(Fig. 6B, 6E)。重组SERPINB3处理上调COL1A1、TGFβ1、CitH3,而这些效应可被Metelimumab逆转(Fig. 6C, 6F)。AFM和免疫荧光证实rSERPINB3增加血栓硬度和COL1A1沉积,TGFβ1抑制可逆转(Fig. 6G-I)。这些数据共同证明中性粒细胞SERPINB3-TGFβ1-NET-胶原蛋白信号轴通过ROS响应机制增强血栓形成并促进血栓硬化(Fig. 6J)。

图6:中性粒细胞中SERPINB3的表达通过TGFβ1介导的胶原沉积促进血栓硬化
原文链接:https://doi.org/10.1182/blood.2025029516







