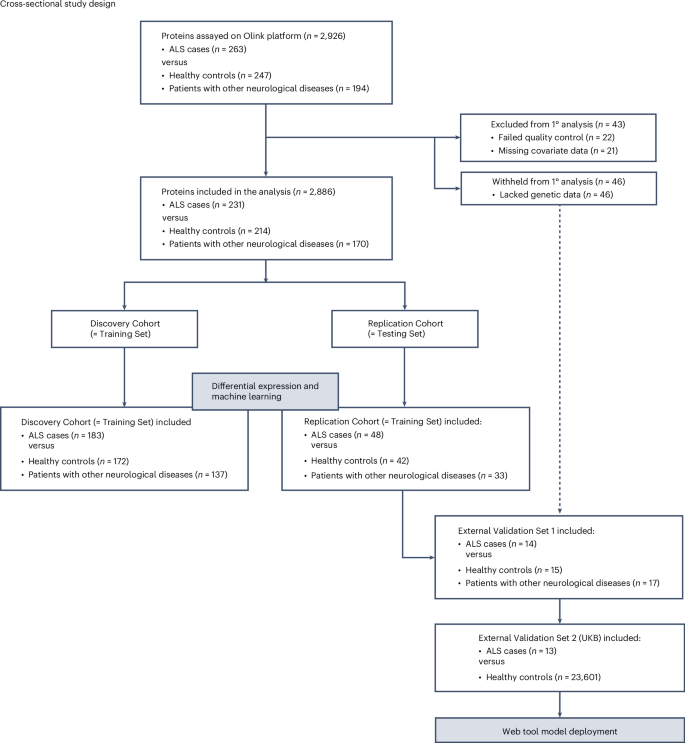
图2 Study workflow.
01
蛋白质标志物的发现
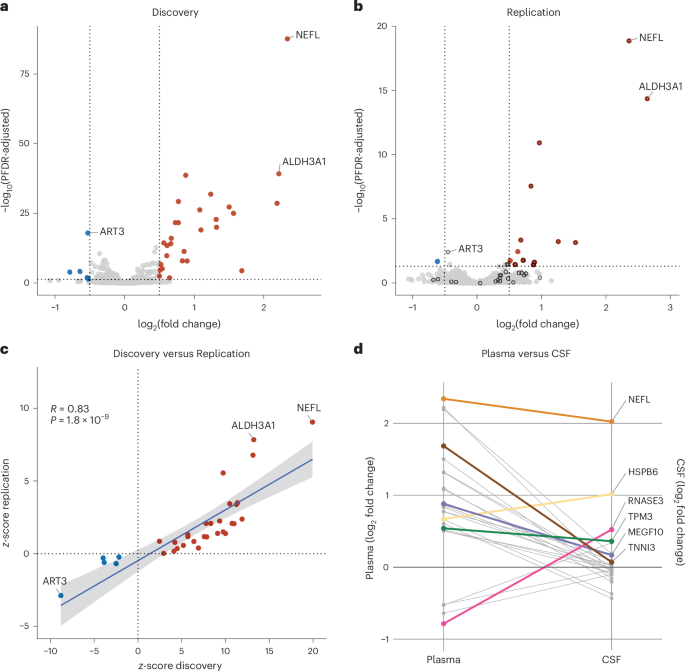
图3 Differential abundance of plasma proteins in patients diagnosed with ALS compared with control individuals.
02
机器学习模型的应用与构建
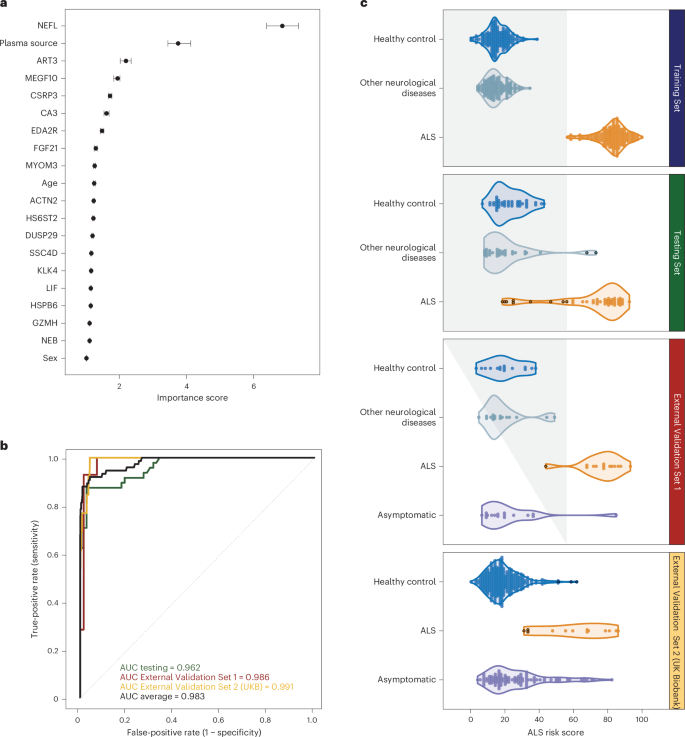
图4 Supervised machine learning to diagnose ALS based on plasma proteins.
03
病前期的生物标志物
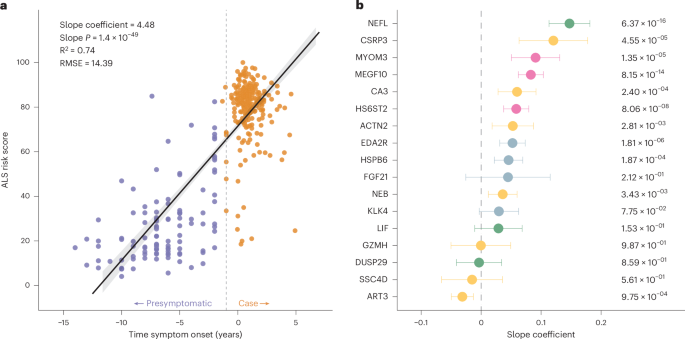
图5 Regression analysis of ALS risk score derived from supervised machine learning predicts the age of ALS onset in asymptomatic patients.
04
ALS与C9orf72扩展的关系
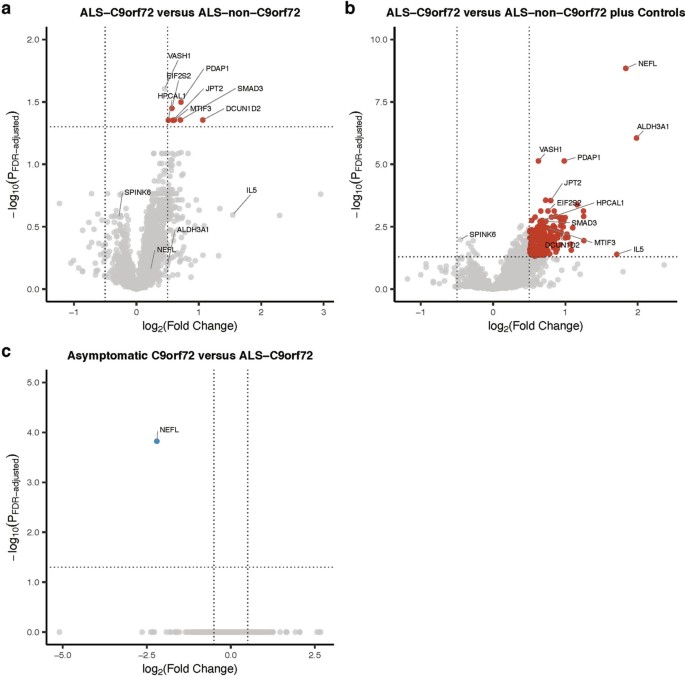
图6 Differential abundance of plasma proteins in ALS patients with C9orf72expansions.
05
小结


图2 Study workflow.
01
蛋白质标志物的发现

图3 Differential abundance of plasma proteins in patients diagnosed with ALS compared with control individuals.
02
机器学习模型的应用与构建

图4 Supervised machine learning to diagnose ALS based on plasma proteins.
03
病前期的生物标志物

图5 Regression analysis of ALS risk score derived from supervised machine learning predicts the age of ALS onset in asymptomatic patients.
04
ALS与C9orf72扩展的关系

图6 Differential abundance of plasma proteins in ALS patients with C9orf72expansions.
05
小结