研究背景
慢性肾脏病(Chronic Kidney Disease, CKD)正悄然影响着全球超过8亿人。由于其早期症状隐匿,这一“沉默进展”的疾病已成为全球增长第三快的致死原因之一。肾纤维化是CKD进展至终末期的共同病理特征,其核心是细胞外基质(ECM)的过度积累。近年研究揭示,ECM不仅是结构支架,更是一个动态的生物信号整合平台,可直接调控细胞命运和代谢状态,并与线粒体稳态密切相关。ECM蛋白1(ECM1)是一种分泌型糖蛋白,在肿瘤中通常扮演促癌角色,但在非癌性疾病中呈现组织特异性作用:它加重心脏纤维化和骨关节炎,却在肝纤维化中表现出保护效应。尽管ECM1在多种疾病中显示出重要性,但其在肾脏,特别是是否通过调控线粒体代谢来影响肾纤维化进程,仍是一个亟待探索的关键科学问题。
2026年3月3日,来自美国康涅狄格大学医学院肾脏病科的周东团队在Nature Metabolism上发表了题为“Early-activated extracellular matrix proteins shape the metabolic and spatial dynamics of the kidney fibrotic microenvironment”的研究论文。本研究旨在系统探究ECM1在CKD早期纤维化中的作用及其调控机制。研究团队整合蛋白质组学、空间转录组学和药物干预等手段,揭示了ECM1作为早期应答的基质蛋白,通过成纤维细胞旁分泌作用于肾小管细胞表面的整合素α2β1受体,激活RhoC-YAP-TEAD4信号轴,进而转录抑制PGC1α介导的线粒体氧化磷酸化(OXPHOS),最终驱动肾纤维化。该研究不仅阐明了ECM1作为连接细胞外基质重塑与线粒体代谢的关键分子,还为CKD的早期诊断和治疗干预提供了新靶点。

文章标题
研究队列与实验设计
动物模型队列(机制研究核心):
◊急性与慢性损伤模型:在小鼠双侧肾脏缺血再灌注损伤(IRI)模型中,于损伤后0、1、4、8、12小时及1、2、3、5、10天等多个时间点收集肾脏样本,用于TMT标记定量蛋白质组学和bulk RNA测序分析,旨在捕捉ECM1的早期动态变化。
◊慢性肾病模型:建立单侧缺血再灌注损伤(IRI)模型(含或不含对侧肾切除)、双侧缺血再灌注损伤模型、单侧输尿管梗阻(UUO)模型、阿霉素(doxorubicin)诱导的肾病模型,以及db/db糖尿病性CKD模型。通过Western Blot和免疫组化等方式验证ECM1在纤维化肾脏中的表达水平及其在肾组织中的定位。
人类临床样本队列(转化研究):收集来自南京中医药大学附属医院的70名健康成人和67名CKD患者的尿液和血清样本。通过ELISA技术检测比较两组人群尿液中ECM1的浓度,并将其与临床指标进行相关性分析,以评估尿液ECM1作为无创诊断标志物的潜力。
细胞与分子机制研究队列:
◊蛋白质组和磷酸化蛋白质组:对AAV9-Scramble和AAV9-Sh Ecm1处理后的纤维化肾脏分别进行全局蛋白质组学和磷酸化蛋白质组学分析,以探寻ECM1下游的信号通路变化。
◊空间转录组学:对成纤维细胞特异性Ecm1敲除小鼠和对照小鼠的纤维化肾脏切片,使用10x Visium平台进行空间转录组测序,结合生物信息学去卷积分析和细胞间通讯分析,在组织原位解析ECM1缺失对纤维化微环境中细胞组成、基因表达空间分布及细胞互作网络的影响。
分子互作与转录调控:利用分子对接技术预测ECM1与整合素的结合模式,并通过免疫共沉淀(Co-IP) 在细胞层面进行验证。通过染色质免疫沉淀-qPCR(ChIP-qPCR) 验证转录因子TEAD4与Pgc1a启动子的结合。
主要研究结果
01. ECM1是肾损伤后早期应答的核心基质蛋白,且其全身性缺失可诱发自发性肾纤维化
通过高分辨率时间序列蛋白质组学分析,研究团队发现ECM1在损伤后4小时内即被快速激活,并于第1天达到表达峰值,而大部分其他基质蛋白则在第10天才显著上调,提示ECM1是纤维化启动的早期事件(图1a-c)。在UUO和db/db糖尿病肾病模型中,ECM1在纤维化肾脏中显著上调,且免疫组化将其定位于肾间质(图1e-h)。临床样本分析显示,CKD患者尿液ECM1水平较健康成人升高约48倍,并与血清肌酐和eGFR显著相关,提示尿液ECM1是潜在的CKD无创诊断标志物(图1i-j)。ECM1全身性敲除小鼠出现自发性肾纤维化,表现为肾功能障碍、肾小管损伤及胶原沉积,证实ECM1对维持肾脏正常结构至关重要(图1l-q)。
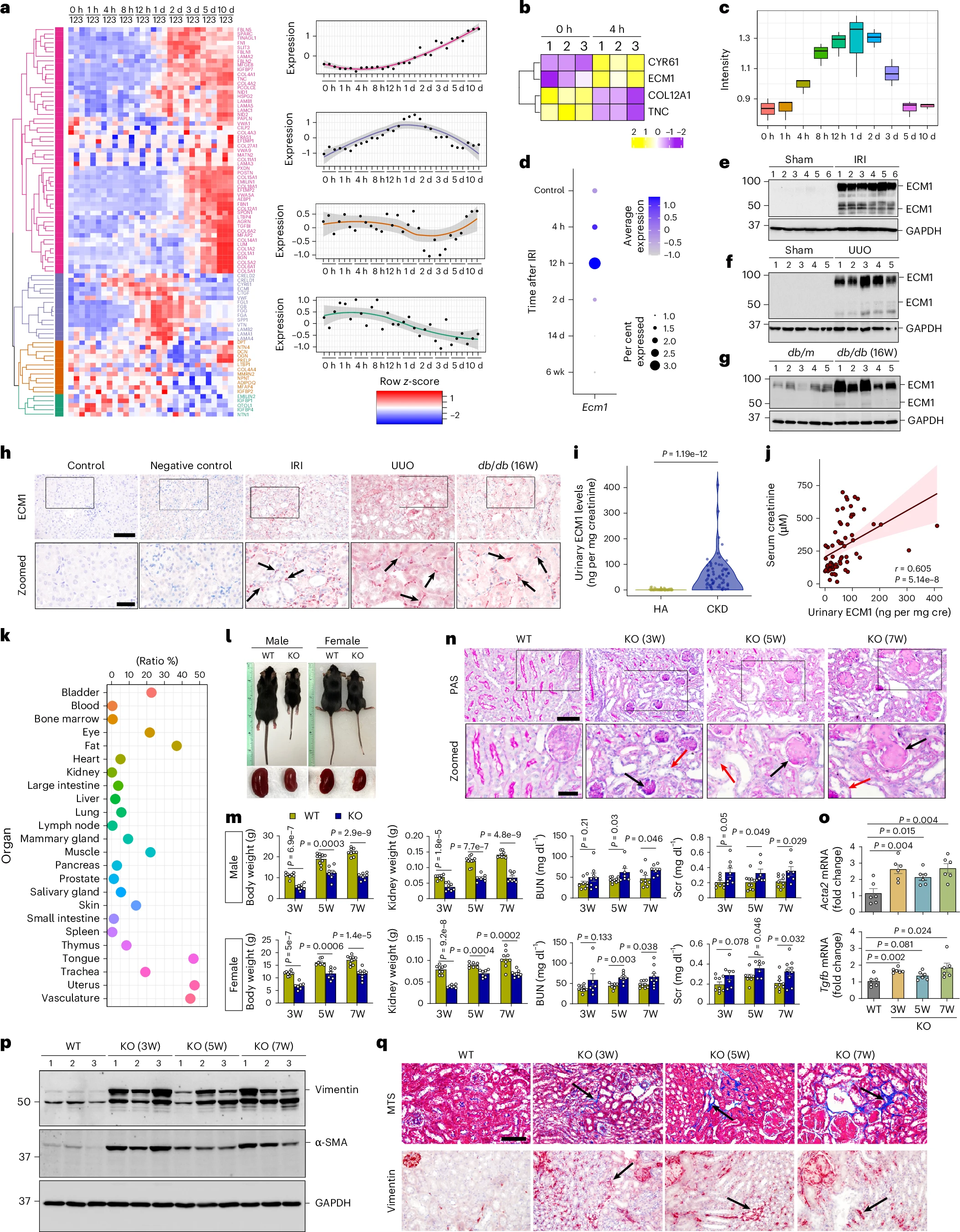
图1:ECM1是CKD中早期激活的核心基质蛋白,而其全身性缺失会导致小鼠自发性肾纤维化
02. 靶向敲低或成纤维细胞特异性敲除ECM1可显著减轻肾纤维化,并伴随线粒体氧化磷酸化增强
为研究ECM1在体内肾纤维化中的功能作用,研究人员利用AAV9-ShEcm1在小鼠体内敲低ECM1,显著减轻了IRI和UUO诱导的肾纤维化,肾功能得到保护,纤维化标志物和胶原沉积减少(图2c-l)。全局蛋白质组学分析发现,ECM1敲降后肾脏中最显著上调的通路是氧化磷酸化(OXPHOS)(图3a-f)。Western Blot和ATP测定证实,线粒体呼吸链复合物I-V蛋白水平和ATP生成在ECM1敲降的纤维化肾脏中均显著升高(图2g-i),透射电镜也观察到线粒体形态更为健康(图2j)。此外,OXPHOS关键调控因子PGC1α及其上游PPARα的蛋白水平也显著上调(图2k)。
为了精准定位ECM1的功能细胞来源,研究者结合单细胞转录组数据分析,发现ECM1在纤维化肾脏中主要来源于成纤维细胞和周细胞。基于这一发现,研究者进一步构建了成纤维细胞特异性(Col1a2-Cre)和周细胞特异性(Pdgfrb-Cre)ECM1敲除小鼠。在这两种细胞特异性敲除小鼠中,IRI或UUO诱导的肾纤维化均被显著抑制,且同样观察到OXPHOS复合物蛋白水平升高和ATP生成增加,与全局敲低实验的表型一致。
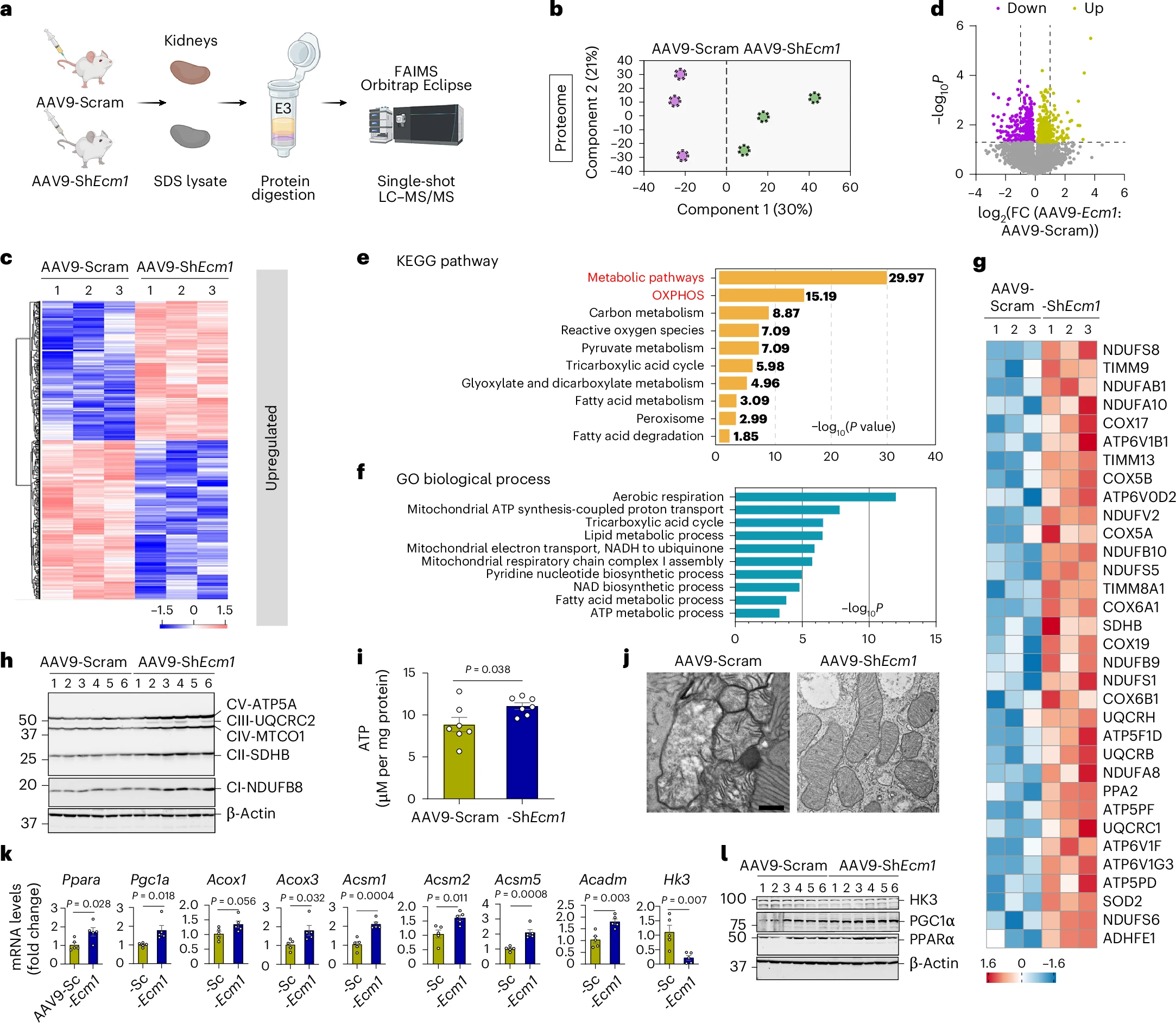
图2:抑制Ecm1可增强纤维化肾脏中的氧化磷酸化(OXPHOS)
03. ECM1通过整合素α2β1-RhoC轴启动信号传递,但其对成纤维细胞自身线粒体无直接影响
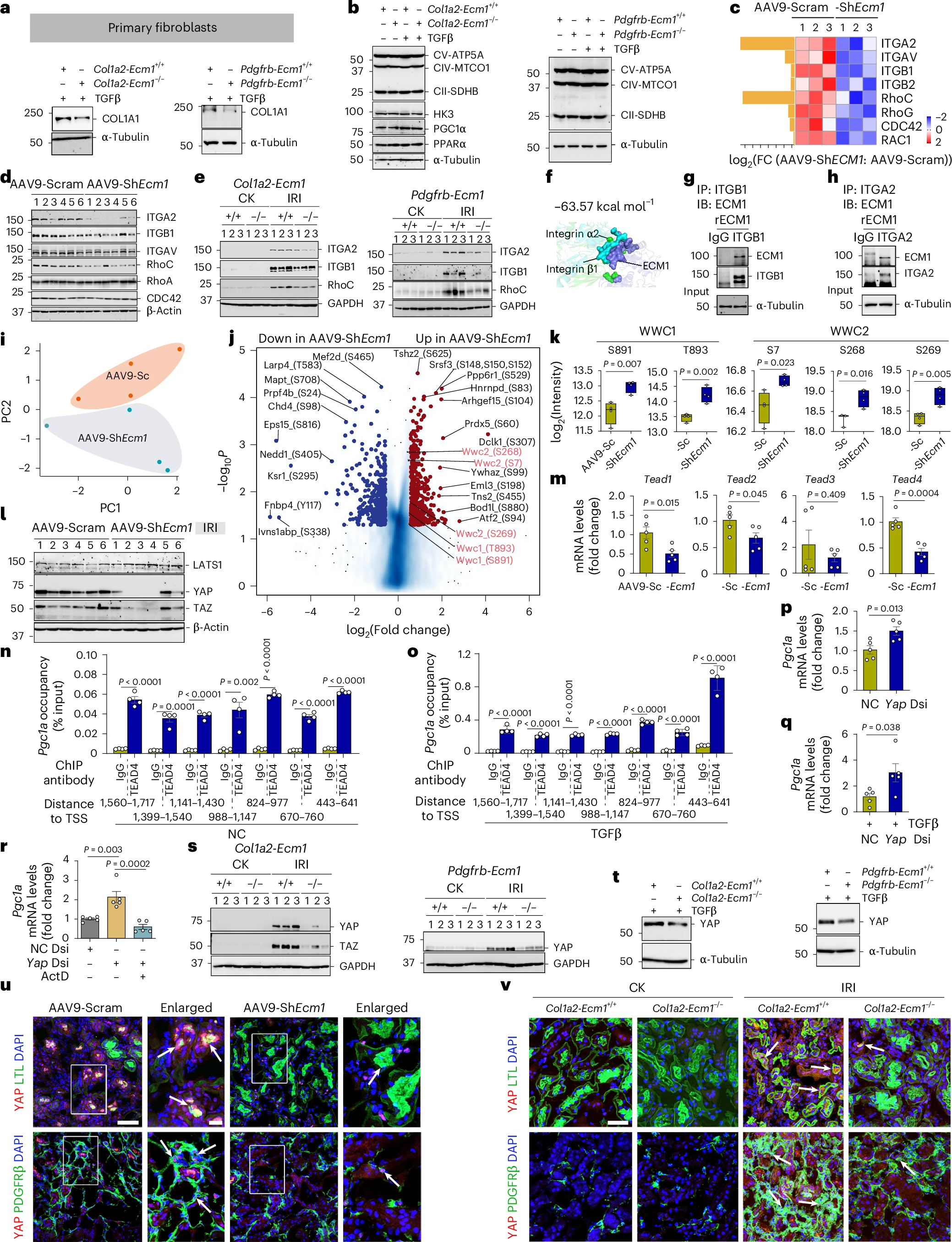
图3:ECM1通过整合素α2β1-RhoC轴启动信号传递
04. 磷酸化蛋白质组学揭示YAP-TEAD4复合物作为关键节点,转录调控PGC1α介导线粒体代谢重编程

图4:磷酸化蛋白质组学揭示,在Ecm1被抑制后的纤维化肾脏中,YAP发生失活
05. 空间转录组学在组织原位证实ECM1缺失重塑纤维化微环境,增强肾小管代谢
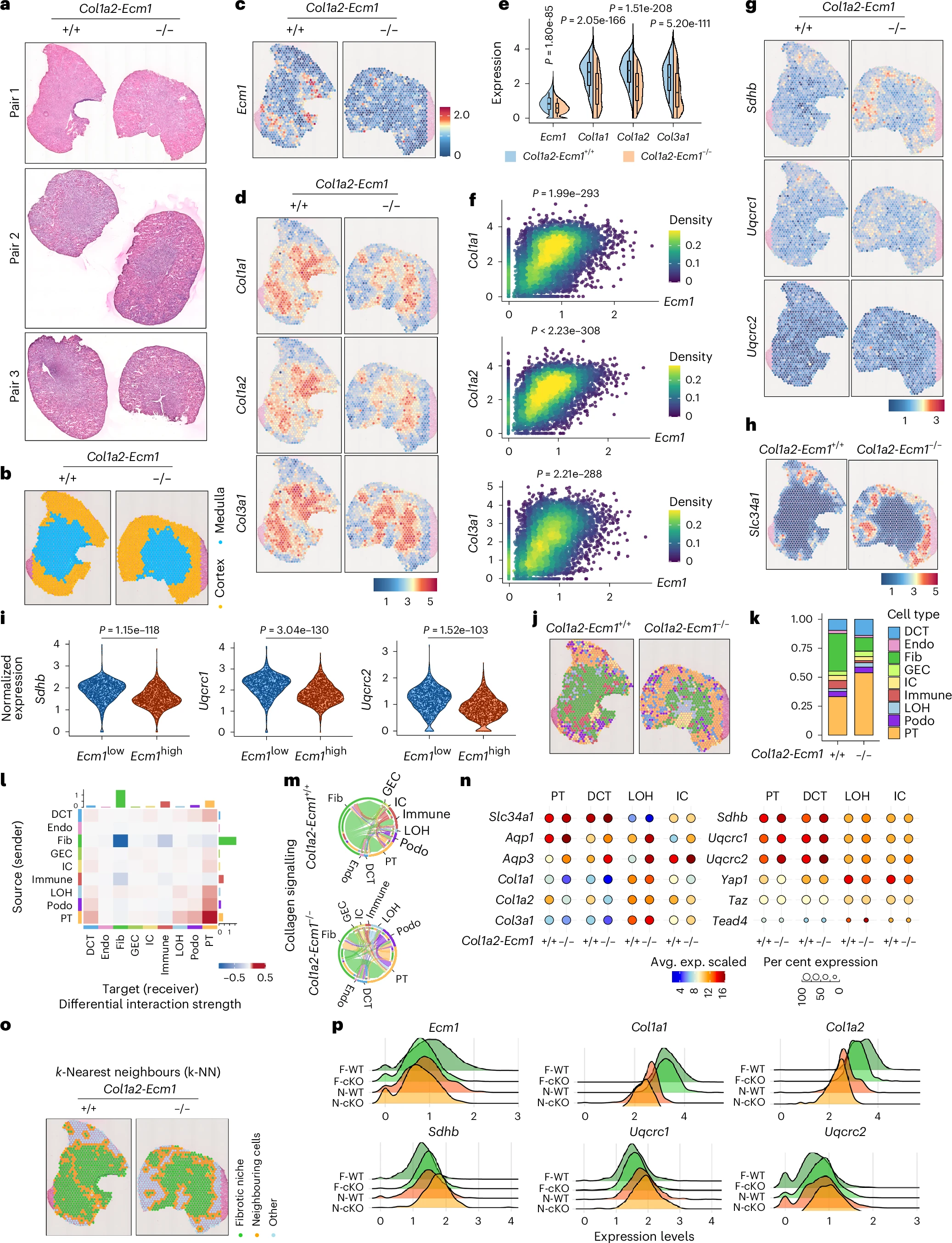
图5:空间转录组学揭示了已形成的纤维化微环境的演变动态
06. 靶向YAP信号通路或直接干预整合素信号,可在体内外模拟ECM1敲除的保护效应
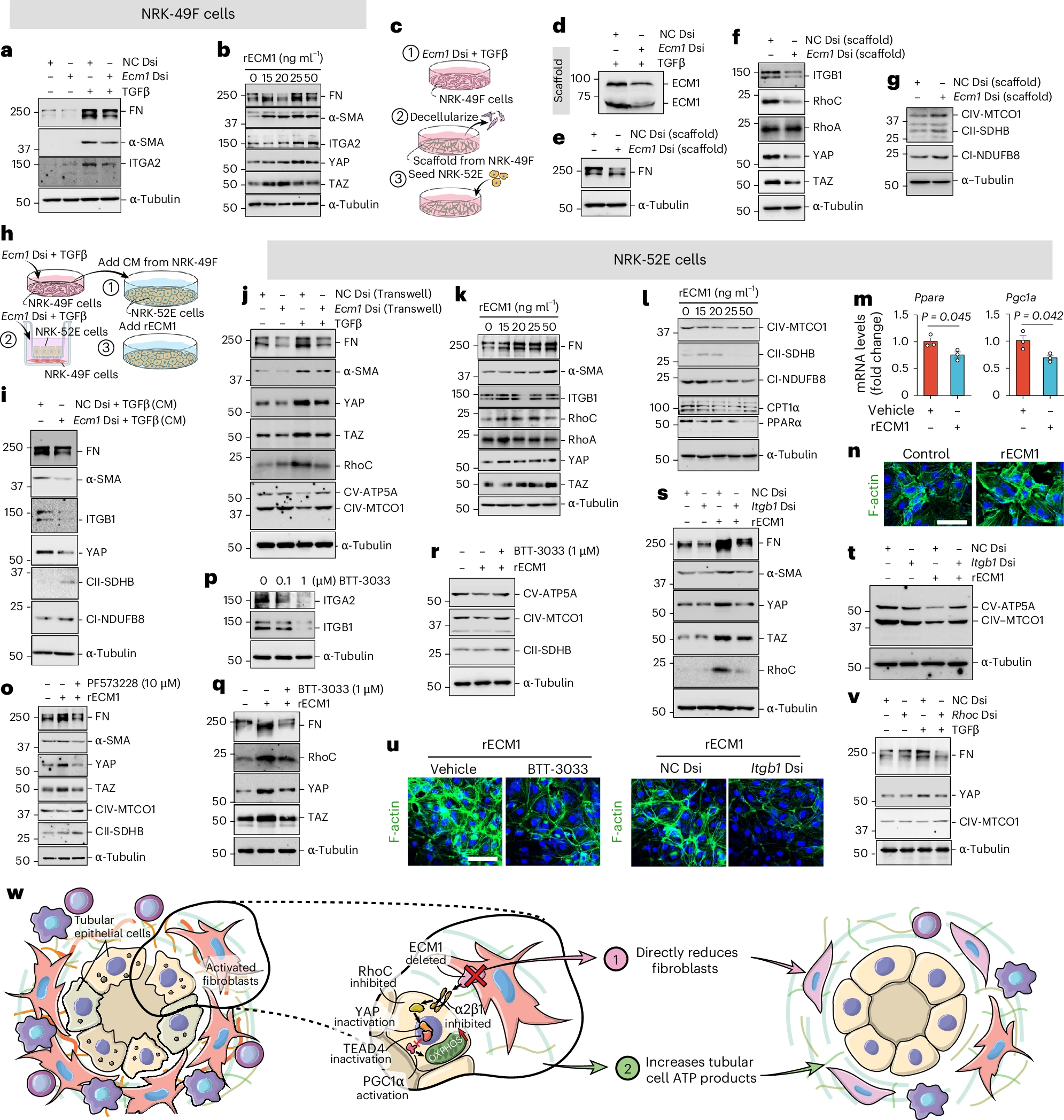
图6:ECM1在离体和体外通过整合素α2β1–RhoC–YAP通路调节线粒体OXPHOS
研究结论
本研究系统阐明了细胞外基质蛋白ECM1在慢性肾脏病早期纤维化中的核心驱动作用及其分子机制。通过多组学分析和功能验证,研究团队发现ECM1是肾损伤后最早应答的基质蛋白之一,其由成纤维细胞分泌,通过旁分泌方式作用于肾小管上皮细胞表面的整合素α2β1受体,激活RhoC-YAP-TEAD4信号轴,进而转录抑制PGC1α,导致线粒体氧化磷酸化功能受损,最终驱动纤维化进程。这一“成纤维细胞-肾小管细胞”跨细胞通讯机制的揭示,将细胞外基质重塑与线粒体代谢重编程这两个关键病理过程有机联系起来,为理解肾纤维化的发生发展提供了全新视角。
原文链接:https://doi.org/10.1038/s42255-026-01458-3
研究背景
慢性肾脏病(Chronic Kidney Disease, CKD)正悄然影响着全球超过8亿人。由于其早期症状隐匿,这一“沉默进展”的疾病已成为全球增长第三快的致死原因之一。肾纤维化是CKD进展至终末期的共同病理特征,其核心是细胞外基质(ECM)的过度积累。近年研究揭示,ECM不仅是结构支架,更是一个动态的生物信号整合平台,可直接调控细胞命运和代谢状态,并与线粒体稳态密切相关。ECM蛋白1(ECM1)是一种分泌型糖蛋白,在肿瘤中通常扮演促癌角色,但在非癌性疾病中呈现组织特异性作用:它加重心脏纤维化和骨关节炎,却在肝纤维化中表现出保护效应。尽管ECM1在多种疾病中显示出重要性,但其在肾脏,特别是是否通过调控线粒体代谢来影响肾纤维化进程,仍是一个亟待探索的关键科学问题。
2026年3月3日,来自美国康涅狄格大学医学院肾脏病科的周东团队在Nature Metabolism上发表了题为“Early-activated extracellular matrix proteins shape the metabolic and spatial dynamics of the kidney fibrotic microenvironment”的研究论文。本研究旨在系统探究ECM1在CKD早期纤维化中的作用及其调控机制。研究团队整合蛋白质组学、空间转录组学和药物干预等手段,揭示了ECM1作为早期应答的基质蛋白,通过成纤维细胞旁分泌作用于肾小管细胞表面的整合素α2β1受体,激活RhoC-YAP-TEAD4信号轴,进而转录抑制PGC1α介导的线粒体氧化磷酸化(OXPHOS),最终驱动肾纤维化。该研究不仅阐明了ECM1作为连接细胞外基质重塑与线粒体代谢的关键分子,还为CKD的早期诊断和治疗干预提供了新靶点。

文章标题
研究队列与实验设计
动物模型队列(机制研究核心):
◊急性与慢性损伤模型:在小鼠双侧肾脏缺血再灌注损伤(IRI)模型中,于损伤后0、1、4、8、12小时及1、2、3、5、10天等多个时间点收集肾脏样本,用于TMT标记定量蛋白质组学和bulk RNA测序分析,旨在捕捉ECM1的早期动态变化。
◊慢性肾病模型:建立单侧缺血再灌注损伤(IRI)模型(含或不含对侧肾切除)、双侧缺血再灌注损伤模型、单侧输尿管梗阻(UUO)模型、阿霉素(doxorubicin)诱导的肾病模型,以及db/db糖尿病性CKD模型。通过Western Blot和免疫组化等方式验证ECM1在纤维化肾脏中的表达水平及其在肾组织中的定位。
人类临床样本队列(转化研究):收集来自南京中医药大学附属医院的70名健康成人和67名CKD患者的尿液和血清样本。通过ELISA技术检测比较两组人群尿液中ECM1的浓度,并将其与临床指标进行相关性分析,以评估尿液ECM1作为无创诊断标志物的潜力。
细胞与分子机制研究队列:
◊蛋白质组和磷酸化蛋白质组:对AAV9-Scramble和AAV9-Sh Ecm1处理后的纤维化肾脏分别进行全局蛋白质组学和磷酸化蛋白质组学分析,以探寻ECM1下游的信号通路变化。
◊空间转录组学:对成纤维细胞特异性Ecm1敲除小鼠和对照小鼠的纤维化肾脏切片,使用10x Visium平台进行空间转录组测序,结合生物信息学去卷积分析和细胞间通讯分析,在组织原位解析ECM1缺失对纤维化微环境中细胞组成、基因表达空间分布及细胞互作网络的影响。
分子互作与转录调控:利用分子对接技术预测ECM1与整合素的结合模式,并通过免疫共沉淀(Co-IP) 在细胞层面进行验证。通过染色质免疫沉淀-qPCR(ChIP-qPCR) 验证转录因子TEAD4与Pgc1a启动子的结合。
主要研究结果
01. ECM1是肾损伤后早期应答的核心基质蛋白,且其全身性缺失可诱发自发性肾纤维化
通过高分辨率时间序列蛋白质组学分析,研究团队发现ECM1在损伤后4小时内即被快速激活,并于第1天达到表达峰值,而大部分其他基质蛋白则在第10天才显著上调,提示ECM1是纤维化启动的早期事件(图1a-c)。在UUO和db/db糖尿病肾病模型中,ECM1在纤维化肾脏中显著上调,且免疫组化将其定位于肾间质(图1e-h)。临床样本分析显示,CKD患者尿液ECM1水平较健康成人升高约48倍,并与血清肌酐和eGFR显著相关,提示尿液ECM1是潜在的CKD无创诊断标志物(图1i-j)。ECM1全身性敲除小鼠出现自发性肾纤维化,表现为肾功能障碍、肾小管损伤及胶原沉积,证实ECM1对维持肾脏正常结构至关重要(图1l-q)。

图1:ECM1是CKD中早期激活的核心基质蛋白,而其全身性缺失会导致小鼠自发性肾纤维化
02. 靶向敲低或成纤维细胞特异性敲除ECM1可显著减轻肾纤维化,并伴随线粒体氧化磷酸化增强
为研究ECM1在体内肾纤维化中的功能作用,研究人员利用AAV9-ShEcm1在小鼠体内敲低ECM1,显著减轻了IRI和UUO诱导的肾纤维化,肾功能得到保护,纤维化标志物和胶原沉积减少(图2c-l)。全局蛋白质组学分析发现,ECM1敲降后肾脏中最显著上调的通路是氧化磷酸化(OXPHOS)(图3a-f)。Western Blot和ATP测定证实,线粒体呼吸链复合物I-V蛋白水平和ATP生成在ECM1敲降的纤维化肾脏中均显著升高(图2g-i),透射电镜也观察到线粒体形态更为健康(图2j)。此外,OXPHOS关键调控因子PGC1α及其上游PPARα的蛋白水平也显著上调(图2k)。
为了精准定位ECM1的功能细胞来源,研究者结合单细胞转录组数据分析,发现ECM1在纤维化肾脏中主要来源于成纤维细胞和周细胞。基于这一发现,研究者进一步构建了成纤维细胞特异性(Col1a2-Cre)和周细胞特异性(Pdgfrb-Cre)ECM1敲除小鼠。在这两种细胞特异性敲除小鼠中,IRI或UUO诱导的肾纤维化均被显著抑制,且同样观察到OXPHOS复合物蛋白水平升高和ATP生成增加,与全局敲低实验的表型一致。

图2:抑制Ecm1可增强纤维化肾脏中的氧化磷酸化(OXPHOS)
03. ECM1通过整合素α2β1-RhoC轴启动信号传递,但其对成纤维细胞自身线粒体无直接影响

图3:ECM1通过整合素α2β1-RhoC轴启动信号传递
04. 磷酸化蛋白质组学揭示YAP-TEAD4复合物作为关键节点,转录调控PGC1α介导线粒体代谢重编程

图4:磷酸化蛋白质组学揭示,在Ecm1被抑制后的纤维化肾脏中,YAP发生失活
05. 空间转录组学在组织原位证实ECM1缺失重塑纤维化微环境,增强肾小管代谢

图5:空间转录组学揭示了已形成的纤维化微环境的演变动态
06. 靶向YAP信号通路或直接干预整合素信号,可在体内外模拟ECM1敲除的保护效应

图6:ECM1在离体和体外通过整合素α2β1–RhoC–YAP通路调节线粒体OXPHOS
研究结论
本研究系统阐明了细胞外基质蛋白ECM1在慢性肾脏病早期纤维化中的核心驱动作用及其分子机制。通过多组学分析和功能验证,研究团队发现ECM1是肾损伤后最早应答的基质蛋白之一,其由成纤维细胞分泌,通过旁分泌方式作用于肾小管上皮细胞表面的整合素α2β1受体,激活RhoC-YAP-TEAD4信号轴,进而转录抑制PGC1α,导致线粒体氧化磷酸化功能受损,最终驱动纤维化进程。这一“成纤维细胞-肾小管细胞”跨细胞通讯机制的揭示,将细胞外基质重塑与线粒体代谢重编程这两个关键病理过程有机联系起来,为理解肾纤维化的发生发展提供了全新视角。
原文链接:https://doi.org/10.1038/s42255-026-01458-3