01 (Nature) 多组学分析揭示健康成年人的年龄相关免疫动态
02 (Cell) 蛋白质限制重编程小鼠衰老的多器官蛋白质组景观
03 (Eur Heart J) 靶向P2Y14R通过PKA/AKAP13/RhoA轴缓解血小板诱导的NET形成和静脉血栓形成
04 (Circulation) 核eNOS与ADAR1相互作用并对其进行S-亚硝基化以调节I型干扰素信号传导和内皮功能
05 (Mol Cancer) IFITM3-MET相互作用通过AKT通路激活驱动EGFR突变非小细胞肺癌奥希替尼耐药
06 (Gastroenterology) 靶向磷脂酰肌醇-3-激酶α/δ和小泛素样修饰因子信号在胰腺癌中的相互依赖性
07 (Gut) 冷动态尿液蛋白质组学整合单细胞和空间转录组学揭示胆管癌肿瘤微环境并预测免疫治疗反应
08 (Ann Rheum Dis) GZMK(+)CD8(+) T细胞靶向干燥综合征中的一种特定腺泡细胞类型
一起来看看本期的蛋白质组学精选优质文献吧!

1. (Nature,IF:50.5) 多组学分析揭示健康成年人的年龄相关免疫动态
2025年10月29日,艾伦免疫学研究所的研究团队发布了一项综合分析健康成年人的免疫系统随年龄变化的多组学研究。该研究对超过300名健康成年人(年龄从25岁到90岁)进行了详细的外周免疫分析,包括单细胞RNA测序、蛋白质组学和流式细胞术。通过这些技术,研究揭示了免疫细胞组成和状态随着年龄的增长发生了显著的变化,特别是在免疫球蛋白和丝氨酸蛋白酶抑制剂等免疫分子水平上的改变。通过对96名成人进行的为期两年的纵向随访,研究团队进一步证明了免疫系统随着年龄和慢性病毒感染的增加发生的逐步退化。
研究结果还发现,T细胞亚群的转录重编程呈现非线性变化,且这种重编程并不依赖于系统性炎症或慢性巨细胞病毒感染。具体而言,记忆T细胞群体中出现了T辅助2(T(H)2)细胞的偏向,且这一变化与流感疫苗中的抗原反应失调有密切关系。研究表明,免疫系统的这些年龄相关变化可能为疫苗开发和老年免疫健康的干预提供了新的见解。研究团队的工作为我们提供了理解衰老过程中免疫系统变化的重要数据,并为未来的免疫调节和衰老相关疾病的研究提供了新的资源。
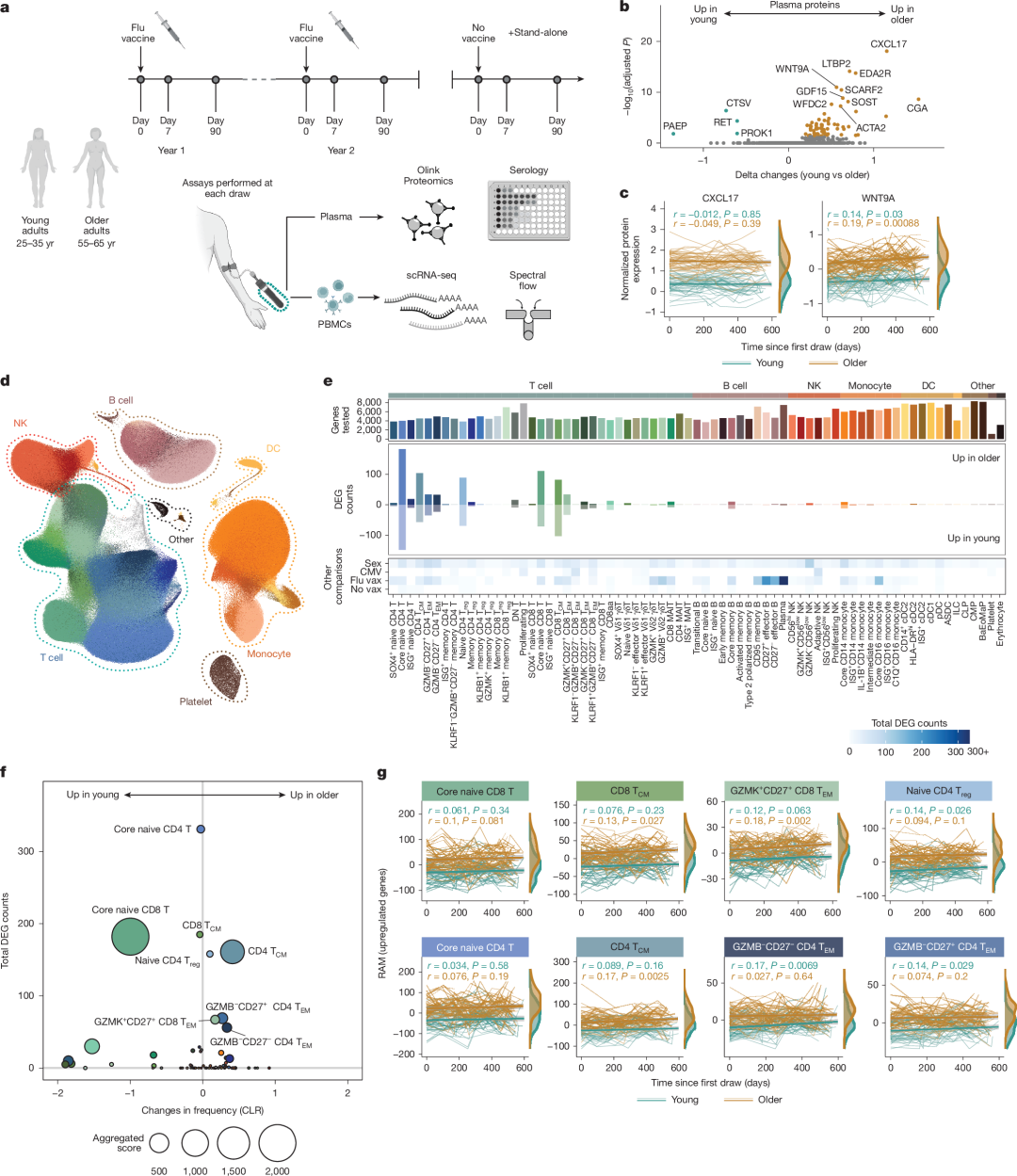
图1 健康人类免疫细胞转录组中与年龄相关的变化。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41162704/

2. (Cell,IF:45.5) 蛋白质限制重编程小鼠衰老的多器官蛋白质组景观
在2025年10月24日,西湖大学生命科学研究院的郭天南教授领导的研究团队发布了一项研究,探讨了蛋白质限制(PR)对衰老过程的影响。这项研究通过对41种小鼠组织进行的全面蛋白质组学分析,揭示了在蛋白质限制条件下,衰老过程中出现的组织特异性变化。研究发现,PR通过减轻与衰老相关的组织特异性蛋白表达、表观基因组状态和磷酸化模式的变化,显著改善了脂肪组织的功能。PR在中年时进行干预最为有效,这一发现为抗衰老的早期干预提供了理论依据。
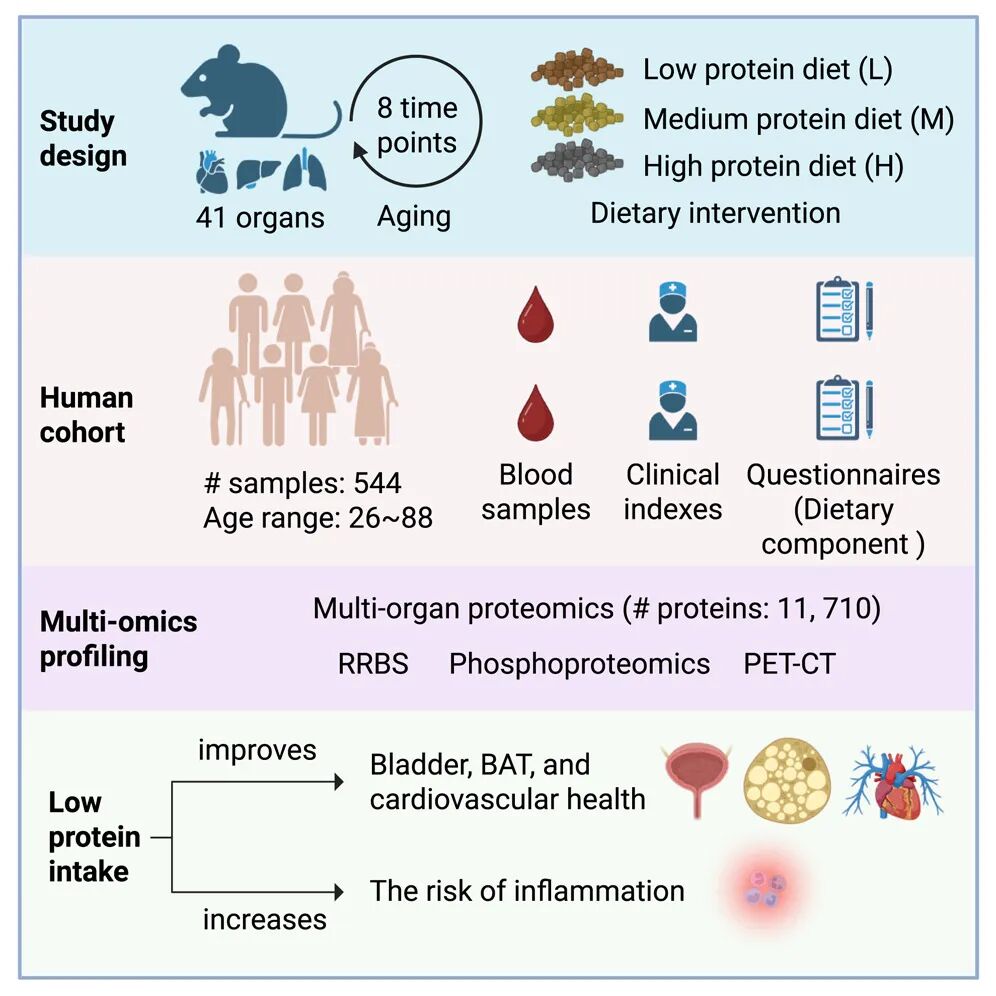
图形摘要。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41138729/

3. (Eur Heart J,IF:37.6) 靶向P2Y14R通过PKA/AKAP13/RhoA轴缓解血小板诱导的NET形成和静脉血栓形成
2025年10月27日,来自中国药科大学的胡庆华教授领导的研究团队在《Eur Heart J》上发表了关于P2Y14受体(P2Y14R)在静脉血栓栓塞症(VTE)中的作用和机制的研究。研究表明,P2Y14R在中性粒细胞上高度表达并参与调节NET(中性粒细胞胞外陷阱)形成。NET的形成不仅加剧了血栓的炎症反应,还与VTE的发生密切相关。通过研究P2Y14R缺陷小鼠,研究发现中性粒细胞特异性P2Y14R缺失可显著减轻小鼠的静脉血栓形成和NET释放。
进一步的研究揭示,P2Y14R通过激活PKA/AKAP13/RhoA信号通路来促进中性粒细胞-血小板聚集和NET的释放。该机制的抑制有望成为新的抗血栓治疗策略。研究还通过高通量药物筛选,鉴定出丙谷胺是一种有效的P2Y14R拮抗剂,能够有效减轻血栓和NET的形成。这项研究为VTE的治疗提供了新的靶点和治疗策略,进一步拓展了血栓相关疾病的治疗方案。
原文链接:
https://pubmed.ncbi.nlm.nih.gov/41143464/

4. (Circulation,IF:35.5) 核eNOS与ADAR1相互作用并对其进行S-亚硝基化以调节I型干扰素信号传导和内皮功能
法兰克福大学分子医学中心的Ingrid Fleming教授及其团队于2025年10月29日发布了一项关于核内一氧化氮合酶(eNOS)在内皮细胞功能中的新作用的研究。研究发现,eNOS不仅局限于细胞膜或高尔基体,还在内皮细胞核中发挥重要作用,并通过与双链RNA特异性腺苷脱氨酶(ADAR1)的相互作用来调节I型干扰素信号通路。eNOS通过S-亚硝基化作用改变ADAR1的功能,进而影响细胞周期基因的表达和细胞增殖。
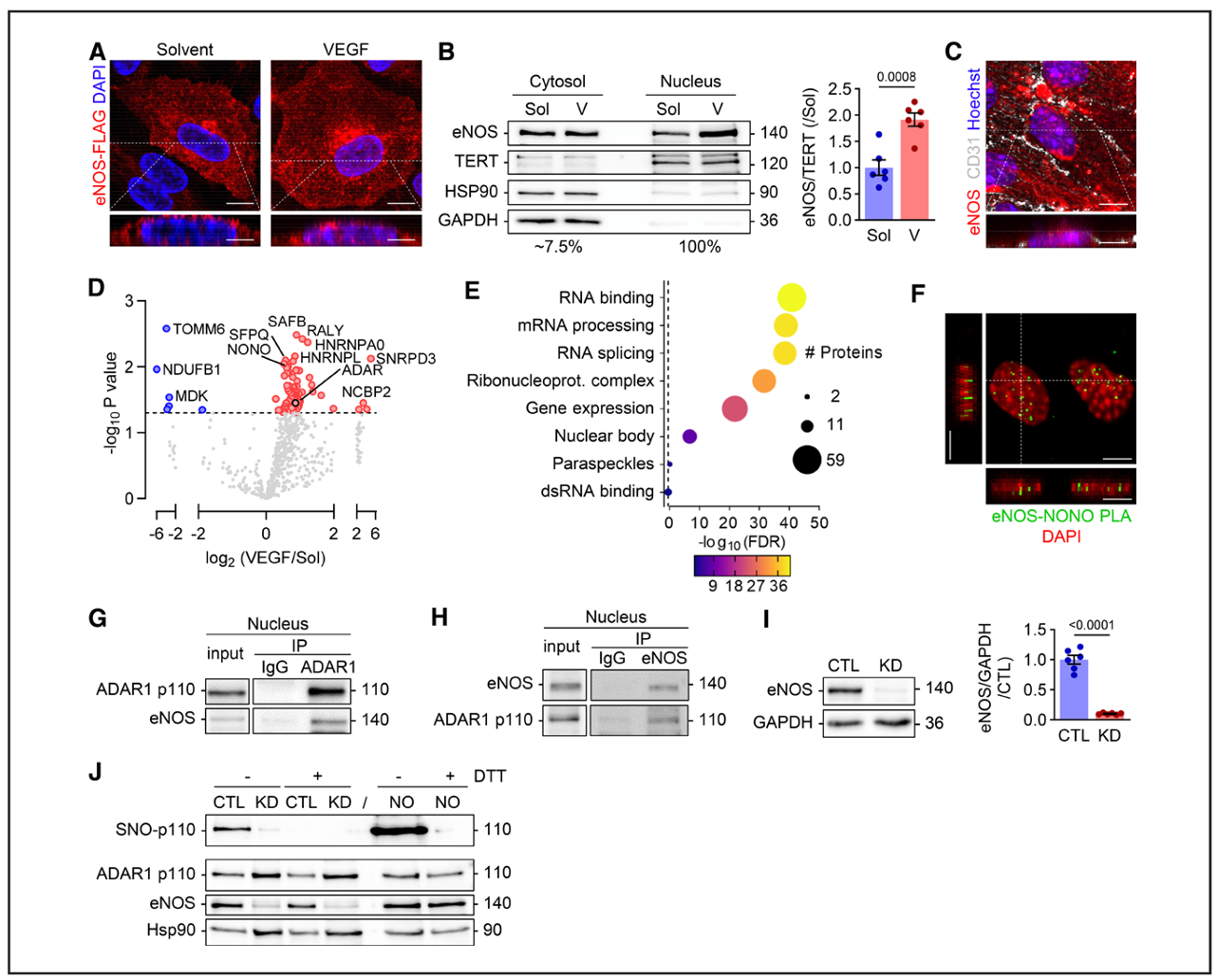
图1 核eNOS与RNA结合蛋白相互作用并对ADAR1进行S-亚硝基化。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41159282/

5. (Mol Cancer,IF:27.7) IFITM3-MET相互作用通过AKT通路激活驱动EGFR突变非小细胞肺癌奥希替尼耐药
九州大学医学院的Okamoto Isamu教授领导的研究团队于2025年10月28日发布了关于EGFR突变非小细胞肺癌(NSCLC)奥希替尼耐药的分子机制研究。该研究发现,尽管对 EGFR‑突变非小细胞肺癌(NSCLC)患者而言,使用 Osimertinib(奥希替尼)作为 EGFR 酪氨酸激酶抑制剂(EGFR‑TKI)治疗时,通常能够在初期取得良好的疗效,但随着治疗时间延长,几乎所有患者最终都会出现耐药,导致疗效丧失。研究表明,IFITM3在奥希替尼耐药的NSCLC患者中上调,并通过与MET的相互作用激活AKT信号通路,从而促进了耐药的发生。
研究团队通过对临床样本和细胞系的深入分析,揭示了肿瘤微环境(TME)衍生的细胞因子促使IFITM3表达增加,从而激活了AKT通路,导致耐药性发展。进一步的实验发现,联合使用MET抑制剂可以有效抑制奥希替尼耐药的发生,显示出这一策略的治疗潜力。这项研究为改善EGFR突变NSCLC的治疗效果提供了新的治疗思路和策略。
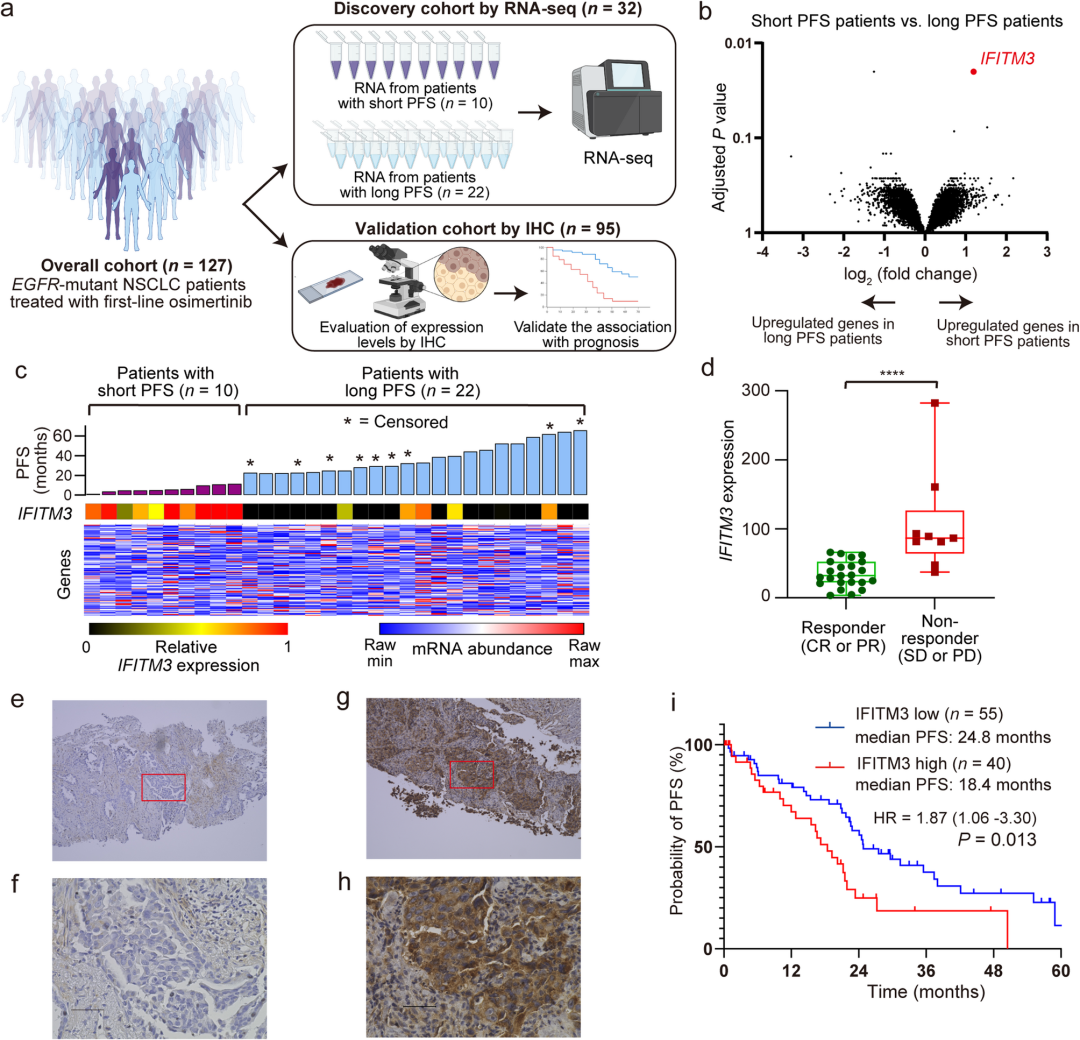
图1 IFITM3表达与EGFR突变型非小细胞肺癌(NSCLC)不良临床结果相关。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41152910/

6. (Gastroenterology,IF:25.7) 靶向磷脂酰肌醇-3-激酶α/δ和小泛素样修饰因子信号在胰腺癌中的相互依赖性
慕尼黑工业大学的Matthias Wirth教授领导的研究团队于2025年10月27日发布了一项关于胰腺癌(PDAC)中PI3K和SUMO通路相互依赖性的研究。该研究发现,PI3K信号通路在PDAC的发展和维持中起着关键作用,且与SUMO通路之间存在相互依赖性。通过基因和药理学筛选,研究团队揭示了双重靶向PI3Kα/δ和SUMO通路能够诱导合成致死性并显著减少肿瘤生长。
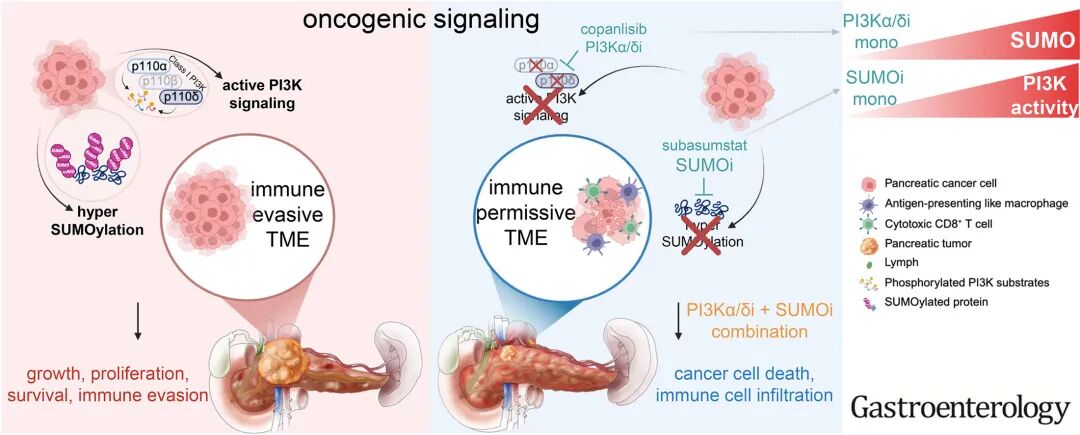
图形摘要
原文链接: https://pubmed.ncbi.nlm.nih.gov/41143762/

7. (Gut,IF:23.0) 动态尿液蛋白质组学整合单细胞和空间转录组学揭示胆管癌肿瘤微环境并预测免疫治疗反应
北京协和医学院医院的赵海涛教授领导的研究团队在2025年10月28日发布了关于胆管癌(BTC)免疫治疗反应预测的研究。该研究结合尿液蛋白质组学、单细胞转录组学和空间转录组学,提出尿液蛋白质组学作为预测免疫治疗反应的新型工具。研究发现,达到免疫治疗持久临床益处的患者表现出免疫激活和全身炎症通路的富集,而没有持久受益的患者则与促肿瘤过程相关。
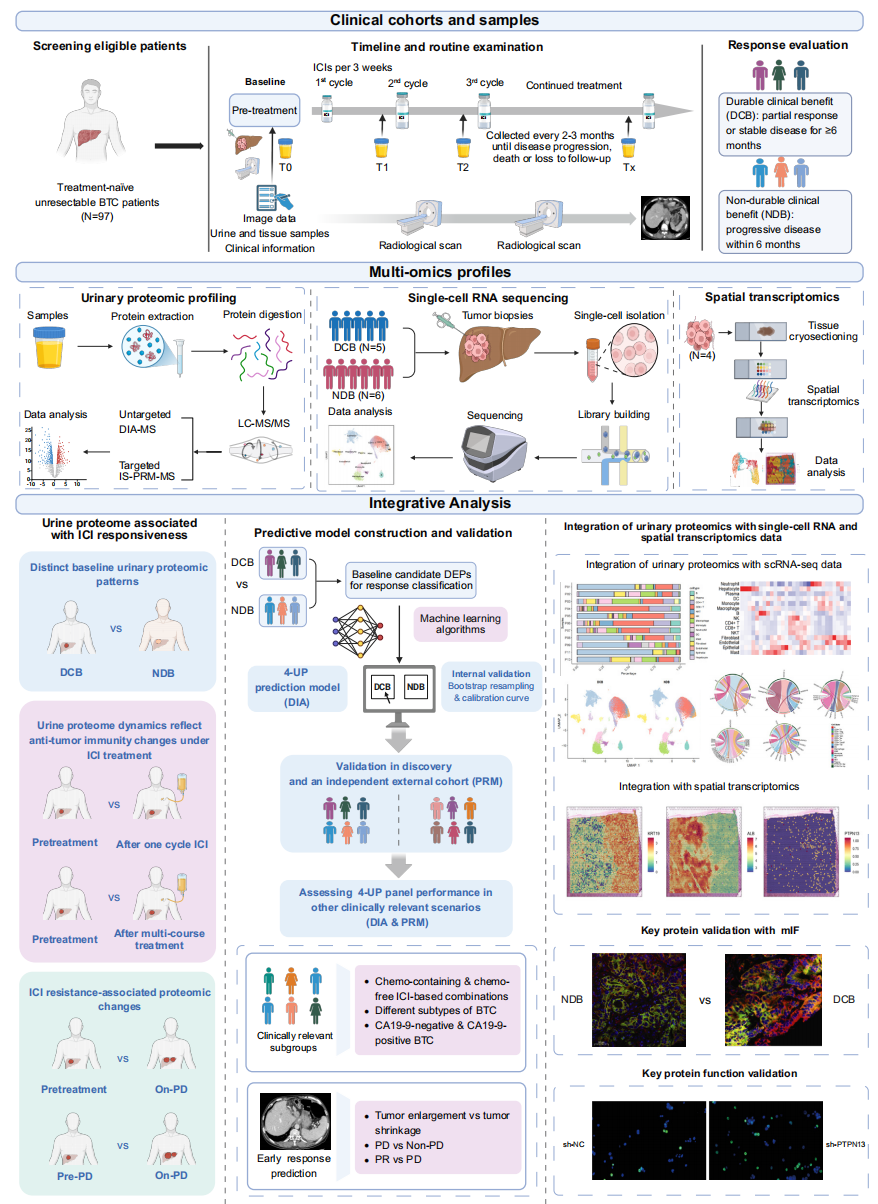
图1 研究设计的示意图。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41151791/

8. (Ann Rheum Dis,IF:20.3) GZMK(+)CD8(+) T细胞靶向干燥综合征中的一种特定腺泡细胞类型
2025年10月28日,美国国立牙科和颅面研究所的Blake M Warner博士领导的研究团队发布了一项关于干燥综合征(SjD)免疫介导机制的新研究。研究发现,GZMK(+)CD8(+) T细胞在干燥综合征患者的唾液腺中显著积累,并通过与腺泡细胞的相互作用,引发上皮细胞的损伤。研究进一步揭示,GZMK(+)CD8(+) T细胞通过干扰素信号传导损害腺泡细胞,导致唾液腺的功能丧失。
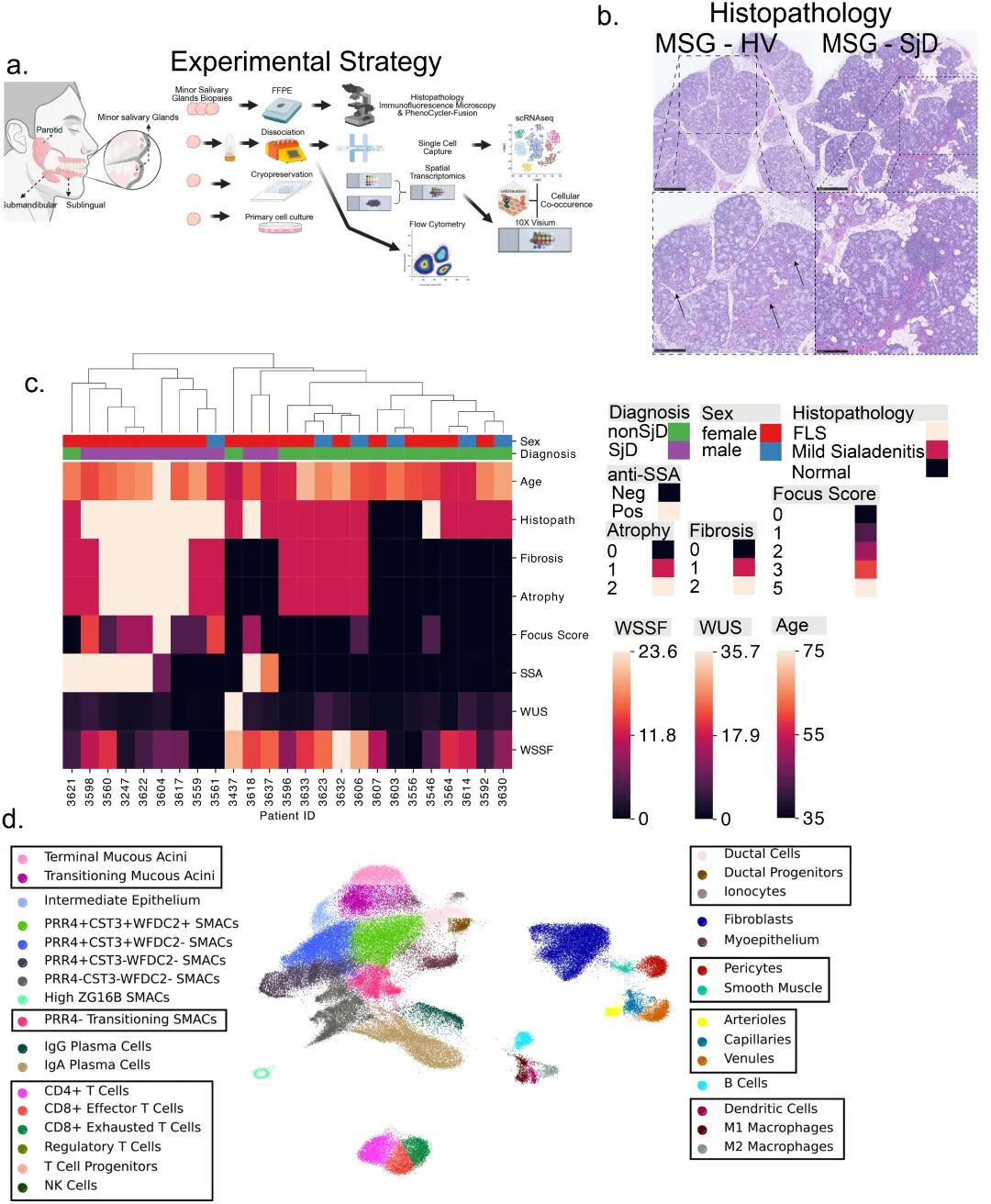
图1. 临床研究对25名受试者进行的调查包括全面的口腔、风湿病学和眼科检查,采用美国风湿病学会2016年干燥综合症分类标准,所有受试者均进行了唾液腺活检。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41162286/
声明:本文内容基于期刊公开信息整理,中文解读及科普文字由多个AI 助手生成,旨在帮助大众快速理解前沿研究,不构成任何专业建议或诊断依据。如需实验或临床应用,请以原始文献与专业人士意见为准。
01 (Nature) 多组学分析揭示健康成年人的年龄相关免疫动态
02 (Cell) 蛋白质限制重编程小鼠衰老的多器官蛋白质组景观
03 (Eur Heart J) 靶向P2Y14R通过PKA/AKAP13/RhoA轴缓解血小板诱导的NET形成和静脉血栓形成
04 (Circulation) 核eNOS与ADAR1相互作用并对其进行S-亚硝基化以调节I型干扰素信号传导和内皮功能
05 (Mol Cancer) IFITM3-MET相互作用通过AKT通路激活驱动EGFR突变非小细胞肺癌奥希替尼耐药
06 (Gastroenterology) 靶向磷脂酰肌醇-3-激酶α/δ和小泛素样修饰因子信号在胰腺癌中的相互依赖性
07 (Gut) 冷动态尿液蛋白质组学整合单细胞和空间转录组学揭示胆管癌肿瘤微环境并预测免疫治疗反应
08 (Ann Rheum Dis) GZMK(+)CD8(+) T细胞靶向干燥综合征中的一种特定腺泡细胞类型
一起来看看本期的蛋白质组学精选优质文献吧!

1. (Nature,IF:50.5) 多组学分析揭示健康成年人的年龄相关免疫动态
2025年10月29日,艾伦免疫学研究所的研究团队发布了一项综合分析健康成年人的免疫系统随年龄变化的多组学研究。该研究对超过300名健康成年人(年龄从25岁到90岁)进行了详细的外周免疫分析,包括单细胞RNA测序、蛋白质组学和流式细胞术。通过这些技术,研究揭示了免疫细胞组成和状态随着年龄的增长发生了显著的变化,特别是在免疫球蛋白和丝氨酸蛋白酶抑制剂等免疫分子水平上的改变。通过对96名成人进行的为期两年的纵向随访,研究团队进一步证明了免疫系统随着年龄和慢性病毒感染的增加发生的逐步退化。
研究结果还发现,T细胞亚群的转录重编程呈现非线性变化,且这种重编程并不依赖于系统性炎症或慢性巨细胞病毒感染。具体而言,记忆T细胞群体中出现了T辅助2(T(H)2)细胞的偏向,且这一变化与流感疫苗中的抗原反应失调有密切关系。研究表明,免疫系统的这些年龄相关变化可能为疫苗开发和老年免疫健康的干预提供了新的见解。研究团队的工作为我们提供了理解衰老过程中免疫系统变化的重要数据,并为未来的免疫调节和衰老相关疾病的研究提供了新的资源。

图1 健康人类免疫细胞转录组中与年龄相关的变化。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41162704/

2. (Cell,IF:45.5) 蛋白质限制重编程小鼠衰老的多器官蛋白质组景观
在2025年10月24日,西湖大学生命科学研究院的郭天南教授领导的研究团队发布了一项研究,探讨了蛋白质限制(PR)对衰老过程的影响。这项研究通过对41种小鼠组织进行的全面蛋白质组学分析,揭示了在蛋白质限制条件下,衰老过程中出现的组织特异性变化。研究发现,PR通过减轻与衰老相关的组织特异性蛋白表达、表观基因组状态和磷酸化模式的变化,显著改善了脂肪组织的功能。PR在中年时进行干预最为有效,这一发现为抗衰老的早期干预提供了理论依据。

图形摘要。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41138729/

3. (Eur Heart J,IF:37.6) 靶向P2Y14R通过PKA/AKAP13/RhoA轴缓解血小板诱导的NET形成和静脉血栓形成
2025年10月27日,来自中国药科大学的胡庆华教授领导的研究团队在《Eur Heart J》上发表了关于P2Y14受体(P2Y14R)在静脉血栓栓塞症(VTE)中的作用和机制的研究。研究表明,P2Y14R在中性粒细胞上高度表达并参与调节NET(中性粒细胞胞外陷阱)形成。NET的形成不仅加剧了血栓的炎症反应,还与VTE的发生密切相关。通过研究P2Y14R缺陷小鼠,研究发现中性粒细胞特异性P2Y14R缺失可显著减轻小鼠的静脉血栓形成和NET释放。
进一步的研究揭示,P2Y14R通过激活PKA/AKAP13/RhoA信号通路来促进中性粒细胞-血小板聚集和NET的释放。该机制的抑制有望成为新的抗血栓治疗策略。研究还通过高通量药物筛选,鉴定出丙谷胺是一种有效的P2Y14R拮抗剂,能够有效减轻血栓和NET的形成。这项研究为VTE的治疗提供了新的靶点和治疗策略,进一步拓展了血栓相关疾病的治疗方案。
原文链接:
https://pubmed.ncbi.nlm.nih.gov/41143464/

4. (Circulation,IF:35.5) 核eNOS与ADAR1相互作用并对其进行S-亚硝基化以调节I型干扰素信号传导和内皮功能
法兰克福大学分子医学中心的Ingrid Fleming教授及其团队于2025年10月29日发布了一项关于核内一氧化氮合酶(eNOS)在内皮细胞功能中的新作用的研究。研究发现,eNOS不仅局限于细胞膜或高尔基体,还在内皮细胞核中发挥重要作用,并通过与双链RNA特异性腺苷脱氨酶(ADAR1)的相互作用来调节I型干扰素信号通路。eNOS通过S-亚硝基化作用改变ADAR1的功能,进而影响细胞周期基因的表达和细胞增殖。

图1 核eNOS与RNA结合蛋白相互作用并对ADAR1进行S-亚硝基化。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41159282/

5. (Mol Cancer,IF:27.7) IFITM3-MET相互作用通过AKT通路激活驱动EGFR突变非小细胞肺癌奥希替尼耐药
九州大学医学院的Okamoto Isamu教授领导的研究团队于2025年10月28日发布了关于EGFR突变非小细胞肺癌(NSCLC)奥希替尼耐药的分子机制研究。该研究发现,尽管对 EGFR‑突变非小细胞肺癌(NSCLC)患者而言,使用 Osimertinib(奥希替尼)作为 EGFR 酪氨酸激酶抑制剂(EGFR‑TKI)治疗时,通常能够在初期取得良好的疗效,但随着治疗时间延长,几乎所有患者最终都会出现耐药,导致疗效丧失。研究表明,IFITM3在奥希替尼耐药的NSCLC患者中上调,并通过与MET的相互作用激活AKT信号通路,从而促进了耐药的发生。
研究团队通过对临床样本和细胞系的深入分析,揭示了肿瘤微环境(TME)衍生的细胞因子促使IFITM3表达增加,从而激活了AKT通路,导致耐药性发展。进一步的实验发现,联合使用MET抑制剂可以有效抑制奥希替尼耐药的发生,显示出这一策略的治疗潜力。这项研究为改善EGFR突变NSCLC的治疗效果提供了新的治疗思路和策略。

图1 IFITM3表达与EGFR突变型非小细胞肺癌(NSCLC)不良临床结果相关。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41152910/

6. (Gastroenterology,IF:25.7) 靶向磷脂酰肌醇-3-激酶α/δ和小泛素样修饰因子信号在胰腺癌中的相互依赖性
慕尼黑工业大学的Matthias Wirth教授领导的研究团队于2025年10月27日发布了一项关于胰腺癌(PDAC)中PI3K和SUMO通路相互依赖性的研究。该研究发现,PI3K信号通路在PDAC的发展和维持中起着关键作用,且与SUMO通路之间存在相互依赖性。通过基因和药理学筛选,研究团队揭示了双重靶向PI3Kα/δ和SUMO通路能够诱导合成致死性并显著减少肿瘤生长。

图形摘要
原文链接: https://pubmed.ncbi.nlm.nih.gov/41143762/

7. (Gut,IF:23.0) 动态尿液蛋白质组学整合单细胞和空间转录组学揭示胆管癌肿瘤微环境并预测免疫治疗反应
北京协和医学院医院的赵海涛教授领导的研究团队在2025年10月28日发布了关于胆管癌(BTC)免疫治疗反应预测的研究。该研究结合尿液蛋白质组学、单细胞转录组学和空间转录组学,提出尿液蛋白质组学作为预测免疫治疗反应的新型工具。研究发现,达到免疫治疗持久临床益处的患者表现出免疫激活和全身炎症通路的富集,而没有持久受益的患者则与促肿瘤过程相关。

图1 研究设计的示意图。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41151791/

8. (Ann Rheum Dis,IF:20.3) GZMK(+)CD8(+) T细胞靶向干燥综合征中的一种特定腺泡细胞类型
2025年10月28日,美国国立牙科和颅面研究所的Blake M Warner博士领导的研究团队发布了一项关于干燥综合征(SjD)免疫介导机制的新研究。研究发现,GZMK(+)CD8(+) T细胞在干燥综合征患者的唾液腺中显著积累,并通过与腺泡细胞的相互作用,引发上皮细胞的损伤。研究进一步揭示,GZMK(+)CD8(+) T细胞通过干扰素信号传导损害腺泡细胞,导致唾液腺的功能丧失。

图1. 临床研究对25名受试者进行的调查包括全面的口腔、风湿病学和眼科检查,采用美国风湿病学会2016年干燥综合症分类标准,所有受试者均进行了唾液腺活检。
原文链接: https://pubmed.ncbi.nlm.nih.gov/41162286/
声明:本文内容基于期刊公开信息整理,中文解读及科普文字由多个AI 助手生成,旨在帮助大众快速理解前沿研究,不构成任何专业建议或诊断依据。如需实验或临床应用,请以原始文献与专业人士意见为准。