研究背景
髓母细胞瘤(Medulloblastoma, MB)作为儿童发病率最高的恶性中枢神经系统肿瘤,其诊疗已进入“分子时代”。虽然手术、化疗与放疗的综合手段大幅提升了生存率,但仍有约 30% 的患儿面临预后不佳的挑战。目前,学界公认 MB 由四个分子亚组构成:WNT、SHH、Group 3(G3)和 Group 4(G4)。它们不仅在基因突变和转录图谱上高度异质,临床表现也截然不同。随着表观遗传和转录组学研究步入成熟期,科研视角正向更深层演进。近年来,蛋白质组学研究的兴起填补了部分功能层面的认知空白,代谢特征(Metabolomics)的系统性分析也处于起步阶段,这为我们提供了从能量代谢重塑角度开发新疗法的可能。
2026年1月15日,法国PSL研究大学Olivier Ayrault 团队与法国、加拿大、美国、德国等多国研究团队合作,在 Cancer Cell 上发表了题为“Multiomic integration reveals tumoral heterogeneity of lipid dependence within lethal group 3 medulloblastoma”的研究论文。
文章标题
本研究基于包含384例原发髓母细胞瘤样本的大型多中心临床队列,整合了甲基化组、转录组、蛋白质组、磷酸化蛋白质组、代谢组等多维度数据,首次系统揭示了G3髓母细胞瘤(尤其是MYC驱动的高危亚型)中脂质代谢的肿瘤异质性。研究发现,MYC在激活脂肪酸合成的同时,还意外地驱动了脂滴形成以储存多余脂质,并通过促进脂滴-线粒体接触为肿瘤细胞供能。研究进一步鉴定出DGAT1为该代谢通路中的关键调控酶,其抑制可诱导肿瘤细胞铁死亡并有效抑制生长,从而为这类难治性脑肿瘤提供了具有潜在转化价值的新代谢靶点。
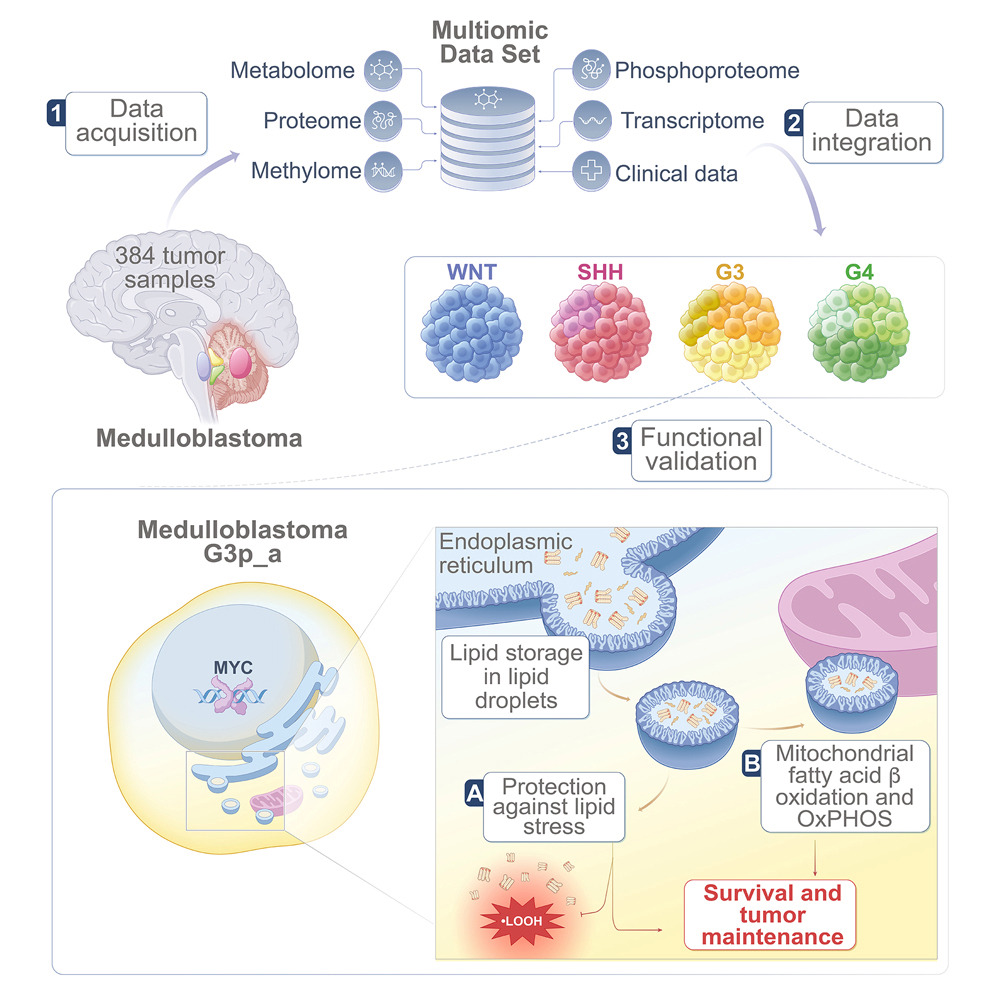
图形摘要
队列设计与实验设计
本研究构建了一个国际多中心队列,共收集了384例原发性髓母细胞瘤患者的快速冷冻肿瘤样本。样本来源于法国、德国、加拿大和美国等多个研究中心,并配对了完整的临床数据(包括年龄、性别、复发状态、转移情况和生存期等)。
研究采用了五层组学数据整合分析:DNA甲基化组(n=369)、转录组(n=341)、蛋白质组(n=343)、磷酸化蛋白质组(n=264)、代谢组(n=170)。
主要研究结果
01. 蛋白质组揭示髓母细胞瘤新的分子亚型结构
通过对大规模蛋白质组数据的无监督聚类分析,在经典的四组分子分型(WNT,SHH,G3,G4)内部,进一步识别出九个稳定的蛋白质组学亚型,包括1个WNT、2个SHH、3个G3和3个G4亚型(Fig. 1C)。这一亚型结构在转录和蛋白层面展现出独特的生物学通路富集(Fig. 1E),特别是在G3髓母细胞瘤中,蛋白质组学分类(G3p_a, G3p_b, G3p_c)比基于甲基化/转录组的SNF分型(G3α, G3β, G3γ)能更清晰地分层患者预后情况(Fig. 2D),突显了蛋白质组学在解析肿瘤功能异质性和预后分层中的关键价值。
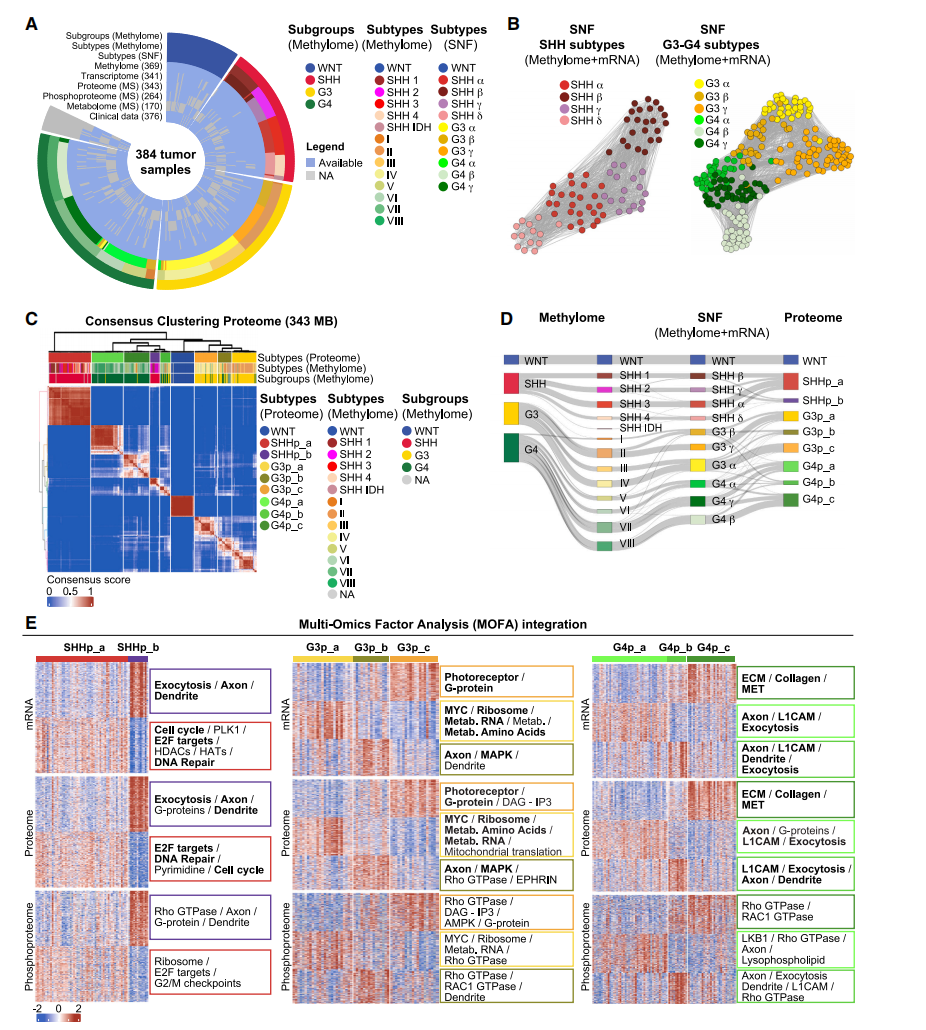
Fig. 1 国际临床注释完善的人髓母细胞瘤多组学队列表征
02. G3p_a亚型表现出独特的脂质富集特征
研究者通过代谢组分析揭示了一个重要发现:在Group 3髓母细胞瘤中,G3p_a亚型表现出明显的脂质代谢重编程(Fig. 2C)。通过无靶向代谢组学检测到的547种代谢物中,有73种在G3亚型间存在差异表达。具体而言,G3p_a肿瘤中长链单不饱和脂肪酸(LC-MUFAs)、长链多不饱和脂肪酸(LC-PUFAs)、单酰甘油和酰基肉碱等脂质种类显著富集。进一步的脂质组学分析证实,G3p_a肿瘤中三酰甘油含量显著升高,而含有饱和脂肪酸或细胞毒性多不饱和脂肪酸的磷脂水平则明显降低(Fig. 2F)。
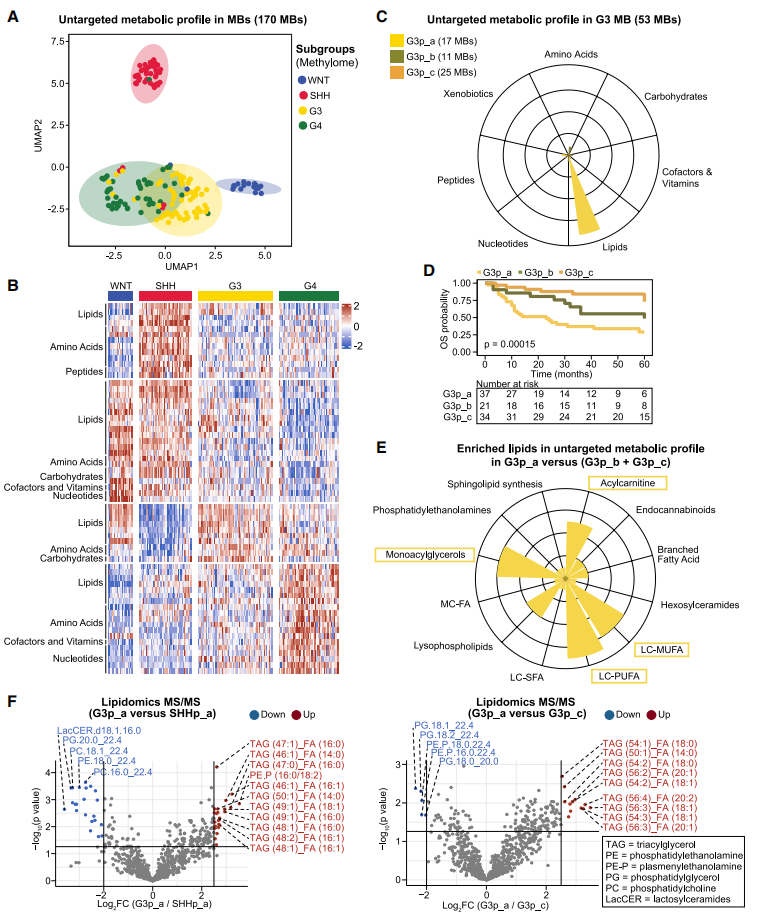
Fig. 2 髓母细胞瘤各亚型的深度代谢谱分析
03. MYC通过DGAT1驱动脂滴形成,将脂质储存与线粒体供能相偶联
为解释G3p_a的脂质表型,研究发现高MYC活性不仅驱动脂肪酸从头合成(FASN/SCD),更重要的是上调了脂滴合成的关键酶DGAT1,促使过量脂肪酸以三酰甘油形式储存于脂滴中(LDs)(Fig. 3A-F)。这些脂滴并非惰性储存,而是通过物理接触与线粒体紧密偶联(Fig. 3L, M),形成代谢单元。脂滴-线粒体互作将储存的脂肪酸输送给线粒体进行β-氧化,从而支持高MYC肿瘤细胞的氧化磷酸化能量需求(Fig. 3H, I, K)。抑制脂滴形成或破坏其与线粒体的连接,会直接损害线粒体呼吸功能,证明这是一种支持肿瘤生长的适应性代谢策略。
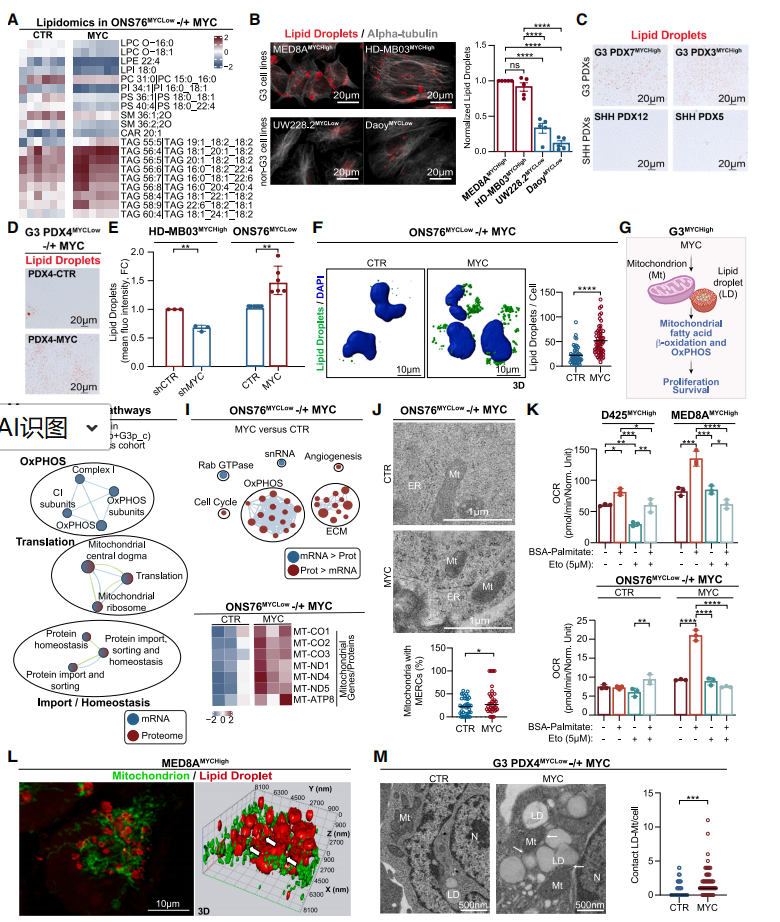
Fig. 3 MYC通过驱动脂滴形成以维持G3MYCHigh肿瘤的线粒体氧化磷酸化
04. 靶向DGAT1通过诱导脂质过氧化与铁死亡,选择性杀伤MYC高表达肿瘤细胞
基于MYC-DGAT1-脂滴轴的机制发现,研究提出靶向脂滴形成酶DGAT1。体外实验表明,在G3p_a细胞模型中,遗传或药理学抑制DGAT1能有效瓦解脂滴,导致未被储存的多不饱和脂肪酸累积并发生脂质过氧化,最终触发铁死亡(Fig. 4I, J)。该死亡过程可被铁死亡抑制剂Ferrostatin-1特异性挽救。重要的是,DGAT1抑制表现出MYC依赖的选择性杀伤,对MYC低表达的肿瘤细胞几乎无效(Fig. 4C),这为精准治疗提供了关键的生物学基础。
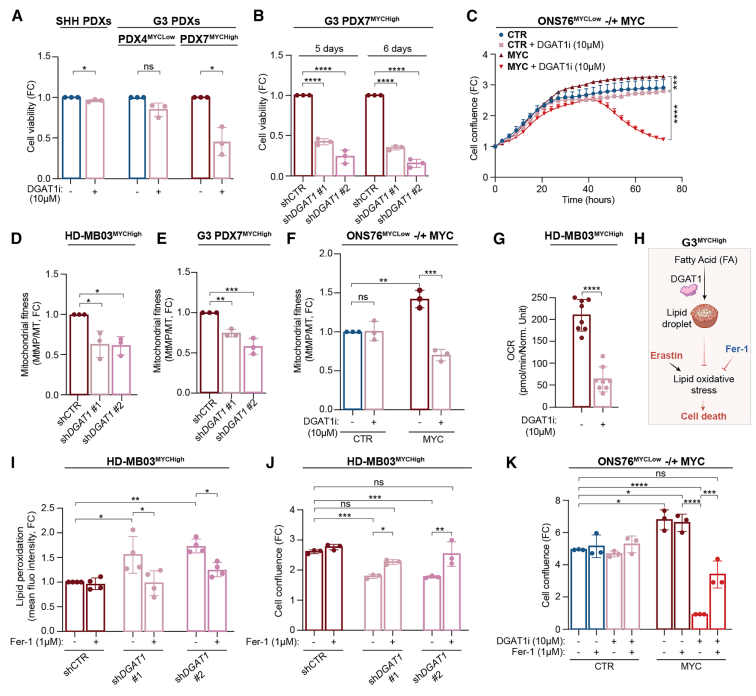
Fig. 4 脂质储存是G3MYCHigh髓母细胞瘤中MYC下游的一个新型脆弱节点
05. 抑制DGAT1在体内有效抑制肿瘤,并与化疗协同增效
体内实验进一步验证了靶向DGAT1的治疗潜力。在原位移植的G3p_a小鼠模型中,敲低或抑制DGAT1能显著减少肿瘤内脂滴、增加脂质过氧化,并有效延长荷瘤小鼠的生存期(Fig. 5A-F)。尤为重要的是,DGAT1抑制剂与标准化疗药物环磷酰胺(CP)联用,在G3p_a模型中表现出强烈的协同抗肿瘤效应(Fig. 5G)。这表明,针对MYC-DGAT1-脂滴轴的靶向治疗,不仅可作为一种单一疗法,更能与现有化疗方案协同,为当前缺乏有效疗法的高危G3髓母细胞瘤(尤其是G3p_a亚型)提供了一种极具前景的新型联合治疗策略。
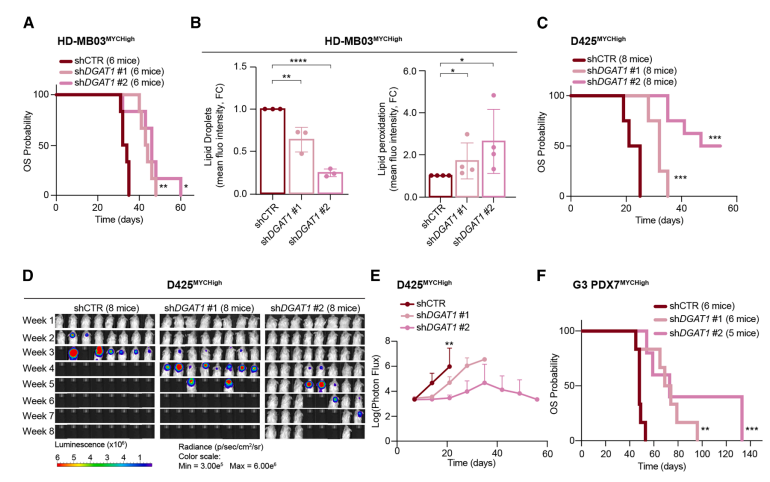
Fig. 5 脂滴对于G3MYCHigh髓母细胞瘤的体内维持至关重要
总结与展望
本研究通过大规模多组学数据整合,首次系统性揭示了MYC 驱动的高危 Group 3肿瘤对脂质储存与利用通路的特异性依赖。研究表明,肿瘤细胞通过增强脂滴形成将过量脂肪酸以 TAG 形式“缓冲”并维持脂质稳态,同时依赖脂滴–线粒体物理与代谢耦联实现脂肪酸动员与氧化供能,从而满足高增殖的能量需求。靶向脂滴合成关键酶 DGAT1 可破坏脂质储存与线粒体稳态,导致脂质过氧化累积并触发铁死亡相关的脂质氧化应激介导细胞死亡,在体内外模型中均呈现显著抗肿瘤效应,并可与标准化疗(如环磷酰胺)形成协同。尽管 DGAT1 抑制剂的入脑效率仍是转化痛点,但本研究揭示的 “MYC–脂滴–线粒体” 轴仍为 G3 髓母细胞瘤提供了潜在的代谢治疗靶点。
原文链接:https://www.sciencedirect.com/science/article/abs/pii/S153561082500546X
研究背景
髓母细胞瘤(Medulloblastoma, MB)作为儿童发病率最高的恶性中枢神经系统肿瘤,其诊疗已进入“分子时代”。虽然手术、化疗与放疗的综合手段大幅提升了生存率,但仍有约 30% 的患儿面临预后不佳的挑战。目前,学界公认 MB 由四个分子亚组构成:WNT、SHH、Group 3(G3)和 Group 4(G4)。它们不仅在基因突变和转录图谱上高度异质,临床表现也截然不同。随着表观遗传和转录组学研究步入成熟期,科研视角正向更深层演进。近年来,蛋白质组学研究的兴起填补了部分功能层面的认知空白,代谢特征(Metabolomics)的系统性分析也处于起步阶段,这为我们提供了从能量代谢重塑角度开发新疗法的可能。
2026年1月15日,法国PSL研究大学Olivier Ayrault 团队与法国、加拿大、美国、德国等多国研究团队合作,在 Cancer Cell 上发表了题为“Multiomic integration reveals tumoral heterogeneity of lipid dependence within lethal group 3 medulloblastoma”的研究论文。

文章标题
本研究基于包含384例原发髓母细胞瘤样本的大型多中心临床队列,整合了甲基化组、转录组、蛋白质组、磷酸化蛋白质组、代谢组等多维度数据,首次系统揭示了G3髓母细胞瘤(尤其是MYC驱动的高危亚型)中脂质代谢的肿瘤异质性。研究发现,MYC在激活脂肪酸合成的同时,还意外地驱动了脂滴形成以储存多余脂质,并通过促进脂滴-线粒体接触为肿瘤细胞供能。研究进一步鉴定出DGAT1为该代谢通路中的关键调控酶,其抑制可诱导肿瘤细胞铁死亡并有效抑制生长,从而为这类难治性脑肿瘤提供了具有潜在转化价值的新代谢靶点。

图形摘要
队列设计与实验设计
本研究构建了一个国际多中心队列,共收集了384例原发性髓母细胞瘤患者的快速冷冻肿瘤样本。样本来源于法国、德国、加拿大和美国等多个研究中心,并配对了完整的临床数据(包括年龄、性别、复发状态、转移情况和生存期等)。
研究采用了五层组学数据整合分析:DNA甲基化组(n=369)、转录组(n=341)、蛋白质组(n=343)、磷酸化蛋白质组(n=264)、代谢组(n=170)。
主要研究结果
01. 蛋白质组揭示髓母细胞瘤新的分子亚型结构
通过对大规模蛋白质组数据的无监督聚类分析,在经典的四组分子分型(WNT,SHH,G3,G4)内部,进一步识别出九个稳定的蛋白质组学亚型,包括1个WNT、2个SHH、3个G3和3个G4亚型(Fig. 1C)。这一亚型结构在转录和蛋白层面展现出独特的生物学通路富集(Fig. 1E),特别是在G3髓母细胞瘤中,蛋白质组学分类(G3p_a, G3p_b, G3p_c)比基于甲基化/转录组的SNF分型(G3α, G3β, G3γ)能更清晰地分层患者预后情况(Fig. 2D),突显了蛋白质组学在解析肿瘤功能异质性和预后分层中的关键价值。

Fig. 1 国际临床注释完善的人髓母细胞瘤多组学队列表征
02. G3p_a亚型表现出独特的脂质富集特征
研究者通过代谢组分析揭示了一个重要发现:在Group 3髓母细胞瘤中,G3p_a亚型表现出明显的脂质代谢重编程(Fig. 2C)。通过无靶向代谢组学检测到的547种代谢物中,有73种在G3亚型间存在差异表达。具体而言,G3p_a肿瘤中长链单不饱和脂肪酸(LC-MUFAs)、长链多不饱和脂肪酸(LC-PUFAs)、单酰甘油和酰基肉碱等脂质种类显著富集。进一步的脂质组学分析证实,G3p_a肿瘤中三酰甘油含量显著升高,而含有饱和脂肪酸或细胞毒性多不饱和脂肪酸的磷脂水平则明显降低(Fig. 2F)。

Fig. 2 髓母细胞瘤各亚型的深度代谢谱分析
03. MYC通过DGAT1驱动脂滴形成,将脂质储存与线粒体供能相偶联
为解释G3p_a的脂质表型,研究发现高MYC活性不仅驱动脂肪酸从头合成(FASN/SCD),更重要的是上调了脂滴合成的关键酶DGAT1,促使过量脂肪酸以三酰甘油形式储存于脂滴中(LDs)(Fig. 3A-F)。这些脂滴并非惰性储存,而是通过物理接触与线粒体紧密偶联(Fig. 3L, M),形成代谢单元。脂滴-线粒体互作将储存的脂肪酸输送给线粒体进行β-氧化,从而支持高MYC肿瘤细胞的氧化磷酸化能量需求(Fig. 3H, I, K)。抑制脂滴形成或破坏其与线粒体的连接,会直接损害线粒体呼吸功能,证明这是一种支持肿瘤生长的适应性代谢策略。

Fig. 3 MYC通过驱动脂滴形成以维持G3MYCHigh肿瘤的线粒体氧化磷酸化
04. 靶向DGAT1通过诱导脂质过氧化与铁死亡,选择性杀伤MYC高表达肿瘤细胞
基于MYC-DGAT1-脂滴轴的机制发现,研究提出靶向脂滴形成酶DGAT1。体外实验表明,在G3p_a细胞模型中,遗传或药理学抑制DGAT1能有效瓦解脂滴,导致未被储存的多不饱和脂肪酸累积并发生脂质过氧化,最终触发铁死亡(Fig. 4I, J)。该死亡过程可被铁死亡抑制剂Ferrostatin-1特异性挽救。重要的是,DGAT1抑制表现出MYC依赖的选择性杀伤,对MYC低表达的肿瘤细胞几乎无效(Fig. 4C),这为精准治疗提供了关键的生物学基础。

Fig. 4 脂质储存是G3MYCHigh髓母细胞瘤中MYC下游的一个新型脆弱节点
05. 抑制DGAT1在体内有效抑制肿瘤,并与化疗协同增效
体内实验进一步验证了靶向DGAT1的治疗潜力。在原位移植的G3p_a小鼠模型中,敲低或抑制DGAT1能显著减少肿瘤内脂滴、增加脂质过氧化,并有效延长荷瘤小鼠的生存期(Fig. 5A-F)。尤为重要的是,DGAT1抑制剂与标准化疗药物环磷酰胺(CP)联用,在G3p_a模型中表现出强烈的协同抗肿瘤效应(Fig. 5G)。这表明,针对MYC-DGAT1-脂滴轴的靶向治疗,不仅可作为一种单一疗法,更能与现有化疗方案协同,为当前缺乏有效疗法的高危G3髓母细胞瘤(尤其是G3p_a亚型)提供了一种极具前景的新型联合治疗策略。

Fig. 5 脂滴对于G3MYCHigh髓母细胞瘤的体内维持至关重要
总结与展望
本研究通过大规模多组学数据整合,首次系统性揭示了MYC 驱动的高危 Group 3肿瘤对脂质储存与利用通路的特异性依赖。研究表明,肿瘤细胞通过增强脂滴形成将过量脂肪酸以 TAG 形式“缓冲”并维持脂质稳态,同时依赖脂滴–线粒体物理与代谢耦联实现脂肪酸动员与氧化供能,从而满足高增殖的能量需求。靶向脂滴合成关键酶 DGAT1 可破坏脂质储存与线粒体稳态,导致脂质过氧化累积并触发铁死亡相关的脂质氧化应激介导细胞死亡,在体内外模型中均呈现显著抗肿瘤效应,并可与标准化疗(如环磷酰胺)形成协同。尽管 DGAT1 抑制剂的入脑效率仍是转化痛点,但本研究揭示的 “MYC–脂滴–线粒体” 轴仍为 G3 髓母细胞瘤提供了潜在的代谢治疗靶点。
原文链接:https://www.sciencedirect.com/science/article/abs/pii/S153561082500546X







