研究背景
EBV⁺弥漫大B细胞淋巴瘤(EBV⁺DLBCL)是一类侵袭性强、预后较差的B细胞恶性肿瘤。传统观点认为,其发生主要与老年相关的免疫衰老有关,但该疾病实际上可见于多个年龄段,提示其致病机制并不能仅用“免疫衰老”来解释。目前,对于EBV⁺DLBCL患者是否存在明确的全身抗病毒免疫缺陷、以及肿瘤微环境如何在空间层面塑造局部免疫抑制状态,仍缺乏系统认识。
近期,利默里克大学医学院研究团队发表题了为《Loss of systemic anti-viral immunity and LMP1-driven suppressive myeloid tumour niches converge to shape the immunobiology of EBV+ diffuse large B-cell lymphoma》 的研究,通过整合外周抗病毒T细胞功能检测、PhenoCycler Fusion(PCF)空间单细胞蛋白组学(原CODEX)以及体外机制模型,系统解析了EBV⁺DLBCL的免疫生物学特征。研究表明,EBV⁺DLBCL并非仅由单一因素驱动,而是全身抗病毒免疫功能受损与LMP1驱动的局部髓系免疫抑制微环境共同作用的结果。

文章标题
队列设计和技术方法
本研究主要包含两类样本和分析体系。
在外周血层面,作者收集了健康供体、EBV阴性DLBCL患者和EBV阳性DLBCL患者的PBMC样本,采用IFN-γ ELISpot 检测T细胞对多种病毒抗原的反应,用于评估机体的系统性抗病毒免疫功能。
在组织层面,作者纳入了EBV阳性和阴性DLBCL、EBV阳性经典霍奇金淋巴瘤(cHL)以及EBV相关传染性单核细胞增多症(IM)的FFPE样本,利用PhenoCycler Fusion平台开展空间单细胞蛋白组学,并结合bulk RNA-seq与体外LMP1诱导模型,进一步解析肿瘤微环境的构成及其潜在形成机制。
研究结果
01. DLBCL患者存在广泛的抗病毒T细胞应答缺陷,且EBV⁺患者更为明显
作者首先利用ELISpot评估外周血PBMC的抗病毒T细胞功能。结果显示,健康供体、EBV阴性DLBCL和EBV阳性DLBCL患者在PHA(植物血凝素)刺激下的总体T细胞反应相近,提示患者并不存在明显的“全局性T细胞功能崩溃”。但在抗原特异性水平上,DLBCL患者的抗病毒免疫应答明显减弱,且这一缺陷在EBV阳性DLBCL中最为突出。这说明DLBCL存在外周免疫异常状态,且在EBV阳性患者中免疫受损状态更为明显。
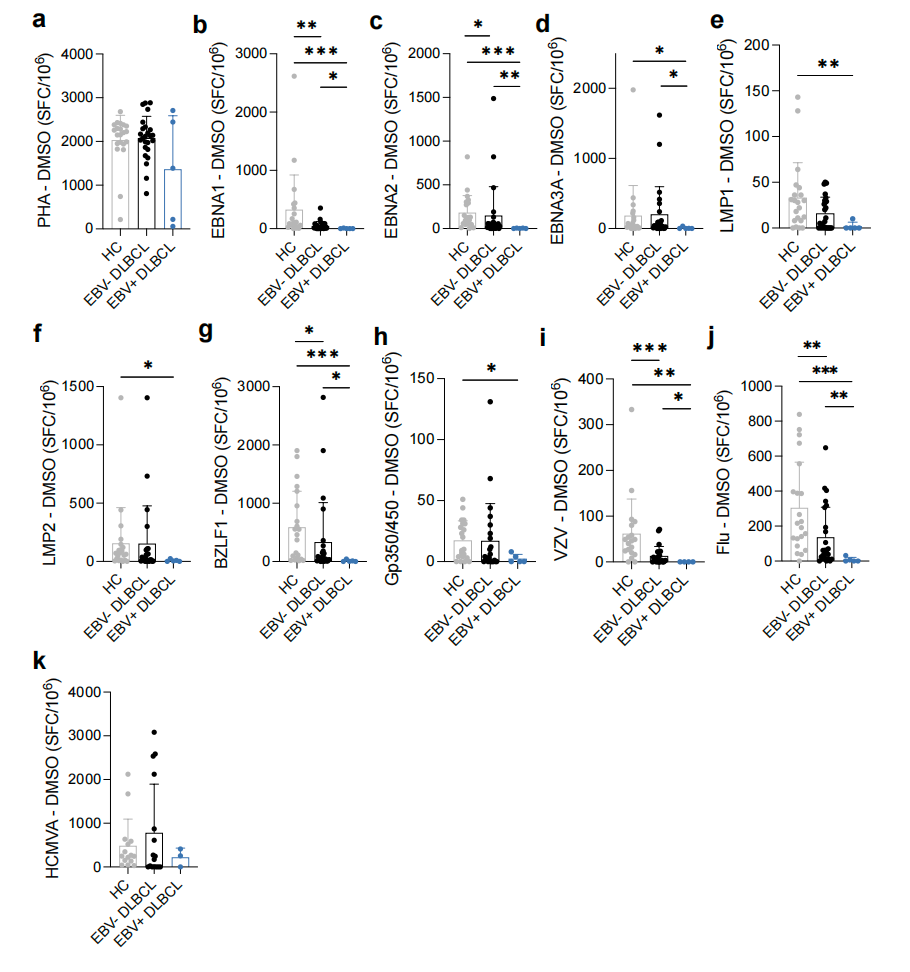
图1 ELISpot抗原应答检测
02. EBV⁺DLBCL并非“免疫细胞少”,而是“免疫浸润增加但细胞毒性CD8⁺T细胞相对不足”
为进一步理解肿瘤局部免疫状态,作者对DLBCL组织开展PCF空间单细胞蛋白组学分析。结果显示,与EBV阴性DLBCL相比,EBV阳性肿瘤中非恶性免疫细胞总体比例更高,肿瘤B细胞比例更低,提示其并不是一个“免疫冷肿瘤”。但更深入分析发现,在全部免疫细胞中,CD8⁺T细胞的相对比例明显下降,而CD4⁺T细胞和Treg比例变化并不显著。这意味着EBV⁺DLBCL虽然整体免疫浸润增多,但真正承担细胞毒性杀伤作用的CD8⁺T细胞却相对匮乏。该现象与外周血中观察到的抗病毒T细胞应答减弱相呼应,提示EBV⁺DLBCL同时存在全身性和局部性T细胞免疫缺陷。
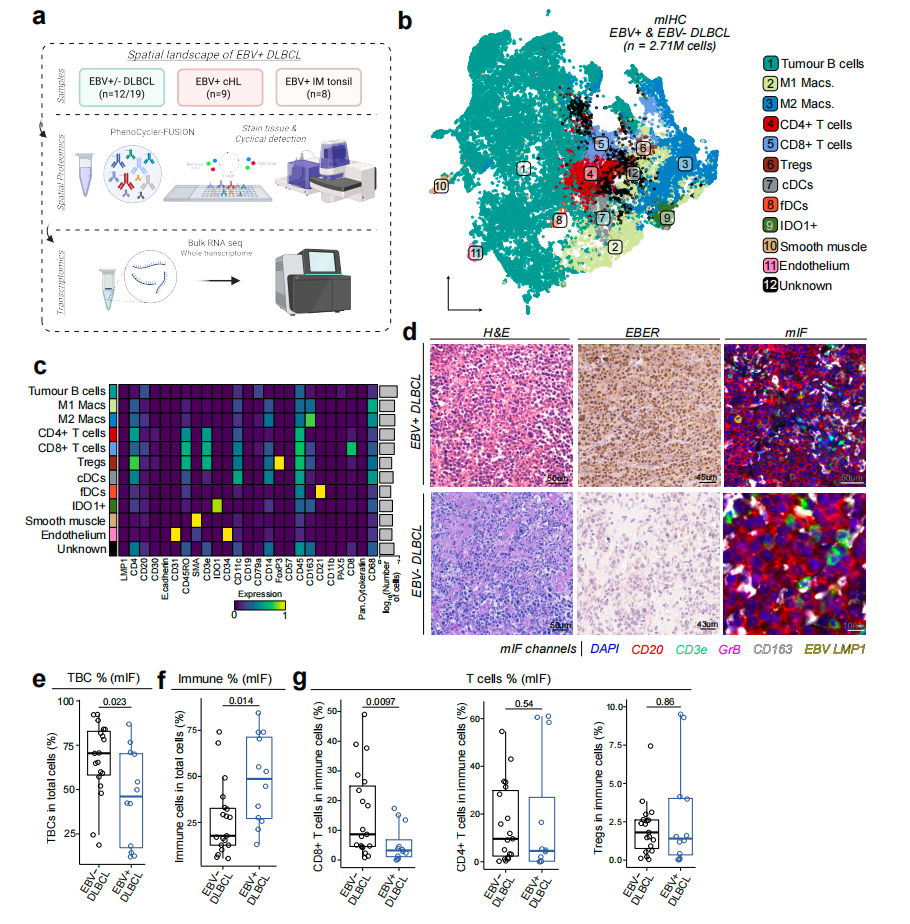
图2 PCF空间蛋白结果
03. 免疫微环境探索
在发现CD8⁺T细胞相对减少后,作者进一步考察了肿瘤中是否存在髓系主导的免疫抑制程序。结果显示,尽管总的M1或M2巨噬细胞数量并未明显升高,但 IDO1⁺ M2-like macrophages 在EBV⁺DLBCL中显著富集,提示其巨噬细胞状态发生了偏向免疫抑制的功能重塑。空间邻域分析进一步发现,这些细胞并非随机分布,而是组织成特定的抑制性细胞邻域。其中,以IDO1⁺巨噬细胞和PD-1⁺Treg富集为特征的抑制性邻域显著扩张,而以CD4⁺和CD8⁺T细胞为主的邻域则明显收缩,说明EBV⁺DLBCL的微环境已经从“效应T细胞主导”转向“髓系抑制主导”。在分子层面,bulk RNA-seq显示EBV⁺DLBCL上调了多种与巨噬细胞免疫调控相关的基因,包括 SPP1、CCL17 等,同时 CCL21 下调,后者通常与T细胞募集和滞留有关。此外,基因集富集分析提示EBV⁺肿瘤富集缺氧相关通路,而缺氧本身已知与SPP1表达升高有关。进一步分析显示,高SPP1表达与较差预后相关。
整体来看,EBV⁺DLBCL呈现出一种巨噬细胞主导、伴随SPP1相关程序增强的免疫抑制微环境,这一生态位很可能参与限制细胞毒性T细胞进入或维持其功能。
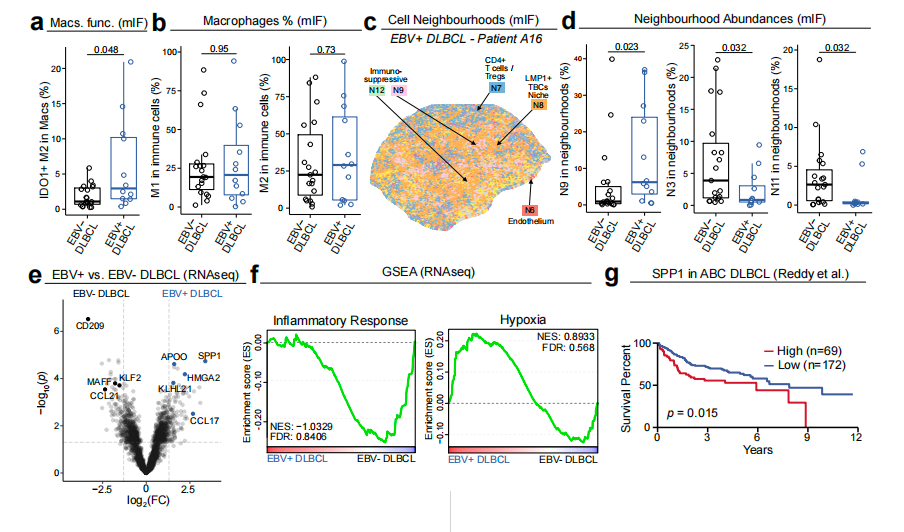
图3 肿瘤微环境分析
04. LMP1表达和细胞微环境
LMP1是EBV编码的重要致癌蛋白,既往已知可影响感染细胞表型并调控趋化因子表达。该研究进一步证实,在原发EBV⁺DLBCL中,LMP1阳性的肿瘤B细胞表现出更独特的表型,包括HLA-DR、HLA-A、PD-L1、CD30、CD44和vimentin表达升高,而CD20表达下降。体外在EBV阴性DLBCL细胞系中诱导LMP1表达后,也可重现上述表型变化,说明这些改变具有较强的LMP1依赖性。更重要的是,空间分析显示,LMP1阳性肿瘤细胞周围显著富集PD-L1⁺ M1-like macrophages以及PD-L1⁺IDO1⁺M2-like 巨噬细胞,形成局部高度抑制性的肿瘤-髓系细胞微区。
进一步研究发现,LMP1表达或EBV感染可诱导DLBCL细胞上调CCL3、CCL5 等单核/巨噬细胞趋化因子,从而为髓系细胞募集提供分子基础。除此之外,LMP1阳性细胞或EBV感染细胞的培养上清还能够诱导THP-1来源巨噬细胞上调 SPP1,提示LMP1不仅能募集髓系细胞,还可能通过旁分泌机制推动其向免疫抑制表型转化。由此可见,LMP1并非仅仅是EBV感染标志物,更可能是EBV⁺DLBCL抑制性肿瘤微环境的核心组织者。
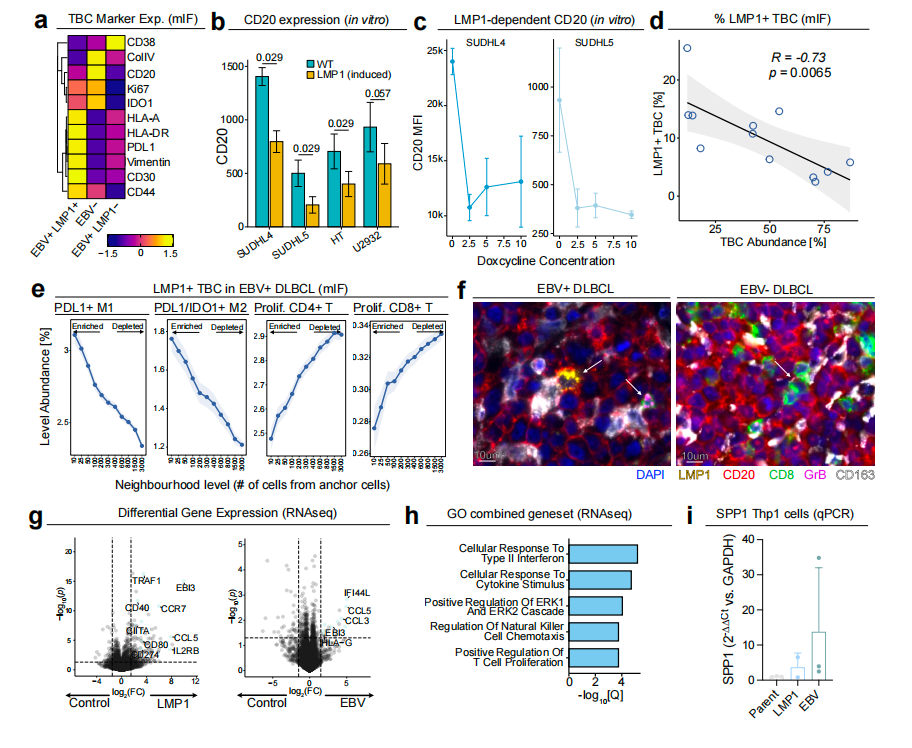
图4 LMP1表达和微环境关系
05. 与其他EBV相关疾病相比,EBV⁺DLBCL表现出最强的免疫抑制和髓系主导特征
为判断上述特征是否为EBV⁺DLBCL 所特有,作者进一步在PCF空间单细胞蛋白结果上将其与EBV 阳性经典霍奇金淋巴瘤(cHL)及传染性单核细胞增多症(IM)进行了比较分析。结果显示,在这三类EBV相关B细胞增殖性疾病中,EBV⁺DLBCL是淋巴细胞最缺乏的一类,其CD4⁺和CD8⁺T细胞丰度均低于cHL和IM。同时,EBV⁺DLBCL中的T细胞表现出更明显的 PD-1高表达,呈现更强的活化/耗竭特征,且相较IM增殖能力更低。进一步围绕LMP1构建的空间分析提示,只有在EBV⁺DLBCL中,LMP1最明显地与致密的PD-L1⁺巨噬细胞聚集、PD-1⁺Treg和T细胞耗竭相关。
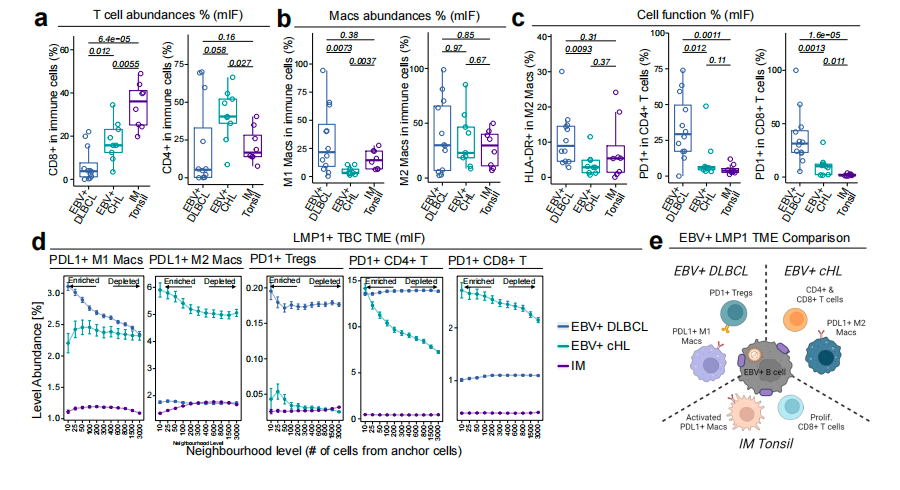
图5 不同EB病毒驱动疾病对比
总结与展望
该研究并未将EBV⁺DLBCL简单归因为老年相关免疫衰老,而是提出了一个更完整的模型:EBV⁺DLBCL的发生发展源于系统性抗病毒T细胞免疫功能受损,与LMP1驱动的局部髓系免疫抑制微环境共同作用。一方面,患者外周存在广泛的抗病毒记忆T细胞功能缺陷;另一方面,肿瘤局部则形成了以PD-L1⁺/IDO1⁺巨噬细胞、PD-1⁺调节/耗竭T细胞以及SPP1相关髓系程序为核心的抑制性生态位,而LMP1在这一过程中发挥了关键组织作用。与其他EBV相关疾病相比,EBV⁺DLBCL展现出更强的免疫抑制和更明确的髓系主导特征。
这些发现不仅深化了对EBV⁺DLBCL免疫生物学的理解,也提示肿瘤细胞—髓系细胞界面可能是未来值得重点关注的干预方向。包括IDO1、SPP1、CCL3/CCL5介导的单核细胞募集以及髓系重编程策略在内的治疗思路,均值得在后续研究中进一步验证。
原文链接:https://www.biorxiv.org/content/10.64898/2026.01.26.701732v1
研究背景
EBV⁺弥漫大B细胞淋巴瘤(EBV⁺DLBCL)是一类侵袭性强、预后较差的B细胞恶性肿瘤。传统观点认为,其发生主要与老年相关的免疫衰老有关,但该疾病实际上可见于多个年龄段,提示其致病机制并不能仅用“免疫衰老”来解释。目前,对于EBV⁺DLBCL患者是否存在明确的全身抗病毒免疫缺陷、以及肿瘤微环境如何在空间层面塑造局部免疫抑制状态,仍缺乏系统认识。
近期,利默里克大学医学院研究团队发表题了为《Loss of systemic anti-viral immunity and LMP1-driven suppressive myeloid tumour niches converge to shape the immunobiology of EBV+ diffuse large B-cell lymphoma》 的研究,通过整合外周抗病毒T细胞功能检测、PhenoCycler Fusion(PCF)空间单细胞蛋白组学(原CODEX)以及体外机制模型,系统解析了EBV⁺DLBCL的免疫生物学特征。研究表明,EBV⁺DLBCL并非仅由单一因素驱动,而是全身抗病毒免疫功能受损与LMP1驱动的局部髓系免疫抑制微环境共同作用的结果。

文章标题
队列设计和技术方法
本研究主要包含两类样本和分析体系。
在外周血层面,作者收集了健康供体、EBV阴性DLBCL患者和EBV阳性DLBCL患者的PBMC样本,采用IFN-γ ELISpot 检测T细胞对多种病毒抗原的反应,用于评估机体的系统性抗病毒免疫功能。
在组织层面,作者纳入了EBV阳性和阴性DLBCL、EBV阳性经典霍奇金淋巴瘤(cHL)以及EBV相关传染性单核细胞增多症(IM)的FFPE样本,利用PhenoCycler Fusion平台开展空间单细胞蛋白组学,并结合bulk RNA-seq与体外LMP1诱导模型,进一步解析肿瘤微环境的构成及其潜在形成机制。
研究结果
01. DLBCL患者存在广泛的抗病毒T细胞应答缺陷,且EBV⁺患者更为明显
作者首先利用ELISpot评估外周血PBMC的抗病毒T细胞功能。结果显示,健康供体、EBV阴性DLBCL和EBV阳性DLBCL患者在PHA(植物血凝素)刺激下的总体T细胞反应相近,提示患者并不存在明显的“全局性T细胞功能崩溃”。但在抗原特异性水平上,DLBCL患者的抗病毒免疫应答明显减弱,且这一缺陷在EBV阳性DLBCL中最为突出。这说明DLBCL存在外周免疫异常状态,且在EBV阳性患者中免疫受损状态更为明显。

图1 ELISpot抗原应答检测
02. EBV⁺DLBCL并非“免疫细胞少”,而是“免疫浸润增加但细胞毒性CD8⁺T细胞相对不足”
为进一步理解肿瘤局部免疫状态,作者对DLBCL组织开展PCF空间单细胞蛋白组学分析。结果显示,与EBV阴性DLBCL相比,EBV阳性肿瘤中非恶性免疫细胞总体比例更高,肿瘤B细胞比例更低,提示其并不是一个“免疫冷肿瘤”。但更深入分析发现,在全部免疫细胞中,CD8⁺T细胞的相对比例明显下降,而CD4⁺T细胞和Treg比例变化并不显著。这意味着EBV⁺DLBCL虽然整体免疫浸润增多,但真正承担细胞毒性杀伤作用的CD8⁺T细胞却相对匮乏。该现象与外周血中观察到的抗病毒T细胞应答减弱相呼应,提示EBV⁺DLBCL同时存在全身性和局部性T细胞免疫缺陷。

图2 PCF空间蛋白结果
03. 免疫微环境探索
在发现CD8⁺T细胞相对减少后,作者进一步考察了肿瘤中是否存在髓系主导的免疫抑制程序。结果显示,尽管总的M1或M2巨噬细胞数量并未明显升高,但 IDO1⁺ M2-like macrophages 在EBV⁺DLBCL中显著富集,提示其巨噬细胞状态发生了偏向免疫抑制的功能重塑。空间邻域分析进一步发现,这些细胞并非随机分布,而是组织成特定的抑制性细胞邻域。其中,以IDO1⁺巨噬细胞和PD-1⁺Treg富集为特征的抑制性邻域显著扩张,而以CD4⁺和CD8⁺T细胞为主的邻域则明显收缩,说明EBV⁺DLBCL的微环境已经从“效应T细胞主导”转向“髓系抑制主导”。在分子层面,bulk RNA-seq显示EBV⁺DLBCL上调了多种与巨噬细胞免疫调控相关的基因,包括 SPP1、CCL17 等,同时 CCL21 下调,后者通常与T细胞募集和滞留有关。此外,基因集富集分析提示EBV⁺肿瘤富集缺氧相关通路,而缺氧本身已知与SPP1表达升高有关。进一步分析显示,高SPP1表达与较差预后相关。
整体来看,EBV⁺DLBCL呈现出一种巨噬细胞主导、伴随SPP1相关程序增强的免疫抑制微环境,这一生态位很可能参与限制细胞毒性T细胞进入或维持其功能。

图3 肿瘤微环境分析
04. LMP1表达和细胞微环境
LMP1是EBV编码的重要致癌蛋白,既往已知可影响感染细胞表型并调控趋化因子表达。该研究进一步证实,在原发EBV⁺DLBCL中,LMP1阳性的肿瘤B细胞表现出更独特的表型,包括HLA-DR、HLA-A、PD-L1、CD30、CD44和vimentin表达升高,而CD20表达下降。体外在EBV阴性DLBCL细胞系中诱导LMP1表达后,也可重现上述表型变化,说明这些改变具有较强的LMP1依赖性。更重要的是,空间分析显示,LMP1阳性肿瘤细胞周围显著富集PD-L1⁺ M1-like macrophages以及PD-L1⁺IDO1⁺M2-like 巨噬细胞,形成局部高度抑制性的肿瘤-髓系细胞微区。
进一步研究发现,LMP1表达或EBV感染可诱导DLBCL细胞上调CCL3、CCL5 等单核/巨噬细胞趋化因子,从而为髓系细胞募集提供分子基础。除此之外,LMP1阳性细胞或EBV感染细胞的培养上清还能够诱导THP-1来源巨噬细胞上调 SPP1,提示LMP1不仅能募集髓系细胞,还可能通过旁分泌机制推动其向免疫抑制表型转化。由此可见,LMP1并非仅仅是EBV感染标志物,更可能是EBV⁺DLBCL抑制性肿瘤微环境的核心组织者。

图4 LMP1表达和微环境关系
05. 与其他EBV相关疾病相比,EBV⁺DLBCL表现出最强的免疫抑制和髓系主导特征
为判断上述特征是否为EBV⁺DLBCL 所特有,作者进一步在PCF空间单细胞蛋白结果上将其与EBV 阳性经典霍奇金淋巴瘤(cHL)及传染性单核细胞增多症(IM)进行了比较分析。结果显示,在这三类EBV相关B细胞增殖性疾病中,EBV⁺DLBCL是淋巴细胞最缺乏的一类,其CD4⁺和CD8⁺T细胞丰度均低于cHL和IM。同时,EBV⁺DLBCL中的T细胞表现出更明显的 PD-1高表达,呈现更强的活化/耗竭特征,且相较IM增殖能力更低。进一步围绕LMP1构建的空间分析提示,只有在EBV⁺DLBCL中,LMP1最明显地与致密的PD-L1⁺巨噬细胞聚集、PD-1⁺Treg和T细胞耗竭相关。

图5 不同EB病毒驱动疾病对比
总结与展望
该研究并未将EBV⁺DLBCL简单归因为老年相关免疫衰老,而是提出了一个更完整的模型:EBV⁺DLBCL的发生发展源于系统性抗病毒T细胞免疫功能受损,与LMP1驱动的局部髓系免疫抑制微环境共同作用。一方面,患者外周存在广泛的抗病毒记忆T细胞功能缺陷;另一方面,肿瘤局部则形成了以PD-L1⁺/IDO1⁺巨噬细胞、PD-1⁺调节/耗竭T细胞以及SPP1相关髓系程序为核心的抑制性生态位,而LMP1在这一过程中发挥了关键组织作用。与其他EBV相关疾病相比,EBV⁺DLBCL展现出更强的免疫抑制和更明确的髓系主导特征。
这些发现不仅深化了对EBV⁺DLBCL免疫生物学的理解,也提示肿瘤细胞—髓系细胞界面可能是未来值得重点关注的干预方向。包括IDO1、SPP1、CCL3/CCL5介导的单核细胞募集以及髓系重编程策略在内的治疗思路,均值得在后续研究中进一步验证。
原文链接:https://www.biorxiv.org/content/10.64898/2026.01.26.701732v1